Ķīmiskā reakcija notiek, kad viena vai vairākas ķīmiskās vielas pārvēršas vienā vai vairākās citās ķīmiskās vielās. Piemēri:
- dzelzs un skābekļa savienošanās, veidojot rūsu.
- etiķis un dzeramā soda apvienojas, veidojot nātrija acetātu, oglekļa dioksīdu un ūdeni.
- degošas vai sprāgstošas lietas.
- daudzas reakcijas, kas notiek dzīvās organismos.
- elektroķīmiskās reakcijas, izlādējot vai uzlādējot akumulatorus.
Dažas reakcijas ir ātras, bet citas - lēnas. Dažas reakcijas notiek dažādos ātrumos atkarībā no temperatūras vai citiem faktoriem. Piemēram, koksne nereaģē ar gaisu, kad tā ir auksta, bet, ja to pietiekami sakarsē, tā sāk degt. Dažas reakcijas izdala enerģiju. Tās ir eksotermiskas reakcijas. Citās reakcijās enerģija tiek uzņemta. Tās ir endotermiskāsreakcijas.
Kodolreakcijas nav ķīmiskas reakcijas. Ķīmiskajās reakcijās ir iesaistīti tikai atomu elektroni; kodolreakcijās ir iesaistīti atomu kodolu protoni un neitroni.
Kas notiek ķīmiskajā reakcijā
Ķīmiskajā reakcijā mainās atomu savienojumi: tiek lauztas vecās ķīmiskās saites un veidotas jaunas. Kopējais atomu skaits saglabājas (masas saglabāšanas likums), tāpēc daudzos iesācēju piemēros reakcijas apraksta ar ķīmiskajām vienādojumiem un stehiometriju — tas palīdz aprēķināt, cik daudz reaģentu vajag un cik produktu rodas.
Galvenie reakciju veidi
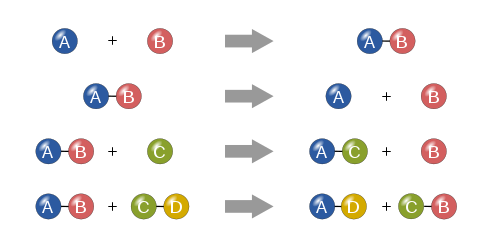
- Sintezes (kombinācijas) reakcijas: divi vai vairāk reaģenti apvienojas, veidojot vienu produktu (A + B → AB).
- Sadalīšanās (dekompozīcijas) reakcijas: viens savienojums sadalās vairākos produktos (AB → A + B).
- Vienvietu apmaiņas reakcijas (single displacement): viens elements izspiež citu no savienojuma (A + BC → AC + B).
- Dubultās apmaiņas reakcijas (double displacement): joni apmainās starp diviem reaģentiem (AB + CD → AD + CB), bieži veidojas nogulsnes vai gāze.
- Redoksreakcijas: tajās notiek elektronu pārvietojums — viens reaģents oksidējas (zaudē elektronus), cits reducējas (uzņem elektronus).
- Skābju-bāzu reakcijas: notiek protonu (H+) pārnešana starp ķīmiskajām vielām (piem., skābe + bāze → sāls + ūdens).
- Degšana (kombustija): ātra eksotermiska oksidēšanās ar liesmas veidošanos, parasti skābekļa klātbūtnē.
Reakcijas ātrumu ietekmējošie faktori
- Temperatūra: paaugstinot temperatūru, daudzas reakcijas norit ātrāk, jo molekulas kustas intensīvāk un biežāk saduras ar nepieciešamo enerģiju.
- Reaģentu koncentrācija: lielāka koncentrācija palielina sadursmju iespējamību, tātad reakcijas ātrumu.
- Virsmas laukums: cietvielu gadījumā smalkāki pulveri reaģē ātrāk nekā lielas daļas.
- Spiediens: gāzveida reaģentiem paaugstināts spiediens līdzvērtīgs lielākai koncentrācijai un var paātrināt reakciju.
- Katalizatori un inhibitori: katalizators samazina nepieciešamo aktivācijas enerģiju un paātrina reakciju, bet inhibitors to palēnina. Bioloģijā katalizatoru lomu bieži pilda enzīmi.
Enerģija, aktivācijas enerģija un reakciju tipiskās īpašības
Eksotermiskas reakcijas izdala siltumu (piem., degšana), bet endotermiskāsreakcijas uzņem siltumu no apkārtējās vides (piem., daži termiski sadalījumi). Lai reakcija notiktu, nepieciešama sākuma enerģija — aktivācijas enerģija — kas ļauj reaģentiem sasniegt pārejas stāvokli. Katalizators samazina šo aktivācijas enerģiju, nemainot galīgo enerģijas bilanci.
Atgriezeniskas reakcijas un ķīmiskā līdzsvara jēdziens
Daudzas reakcijas ir atgriezeniskas — produkti var atkal pārveidoties par reaģentiem. Ja atgriezeniskā reakcija norit vienā un otrā virzienā ar vienādu ātrumu, sistēmā iestājas dinamiskā līdzsvara stāvoklis. Šo stāvokli ietekmē temperatūra, spiediens un koncentrācijas (principu skaidro Le Šatlje likums).
Ķīmiskās reakcijas dzīvībā un tehnoloģijās
Daudzas būtiskas proceses ikdienā un rūpniecībā ir ķīmiskas reakcijas: pārtikas rūpniecībā, medicīnā, enerģētikā, materiālu ražošanā. Dzīvās šūnās ķīmiskas reakcijas notiek kontrolēti un ātri, ko nodrošina enzīmi. Elektroķīmiskās reakcijas, piemēram, notiek akumulatoros un baterijās — tie ir svarīgs enerģijas uzglabāšanas veids.
Drošība un praktiski aspekti
- Strādājot ar reaģentiem, jāievēro drošības noteikumi: aizsargbrilles, cimdi, ventilācija, pareiza glabāšana.
- Degšana un sprādzienbīstamas reakcijas prasa īpašu piesardzību — tās var izdalīt toksiskas gāzes vai radīt ugunsgrēku.
- Rūpnieciskos procesos bieži nepieciešami katalizatori, temperatūras un spiediena kontrole, lai nodrošinātu drošu un efektīvu ražošanu.
Ja vēlaties, varu pievienot vienkāršus ķīmiskos vienādojumus kā paraugus katram reakciju veidam vai paskaidrot, kā aprēķināt reaģentu un produktu masas, izmantojot stehiometriju.