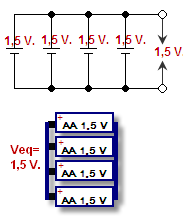
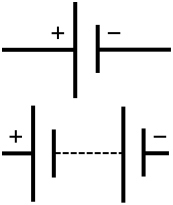Akumulatorā ķīmiskā enerģija tiek pārvērsta elektriskajā enerģijā ķīmiskas reakcijas rezultātā. Parasti ķīmiskās vielas atrodas akumulatora iekšpusē. To izmanto ķēdē, lai darbinātu citus komponentus. Akumulators ražo līdzstrāvas (DC) elektrību (elektrība, kas plūst vienā virzienā un nepārslēdzas uz priekšu un atpakaļ).
Elektrības izmantošana no ēkas kontaktligzdas ir lētāka un efektīvāka, taču akumulators var nodrošināt elektrību vietās, kur nav elektrības sadales. Tā ir noderīga arī lietām, kas pārvietojas, piemēram, elektriskajiem transportlīdzekļiem un mobilajiem tālruņiem.
Akumulatori var būt primārie vai sekundārie. Primārās baterijas tiek izmestas, kad tās vairs nespēj nodrošināt elektrību. Sekundāro var uzlādēt un izmantot atkārtoti.
Darbības princips
Akumulatora darbība balstās uz oksidēšanās-redukcijas (redoks) reakcijām. Tas satur divas elektrodas — anodu (negatīva) un katodu (pozitīva) — un elektrolītu, kas savieno abas puses jonu kustībai. Izlādējoties notiek šādas pamatfāzes:
- Elektroni plūst caur ārējo ķēdi no anodas uz katodu, radot elektrisko strāvu.
- Iekšpusē joni pārvietojas caur elektrolītu, lai saglabātu elektroneitrālumu.
- Ķīmiskās vielas mainās — piemēram, oksidējas vai reducējas — līdz ar enerģijas izsīkumu.
Uzlādes laikā šis process tiek apgriezts ar ārēja strāvas avota palīdzību: ķīmiskās vielas atgūst sākotnējo stāvokli un enerģija tiek uzkrāta.
Akumulatoru galvenās sastāvdaļas un parametri
- Šūnas spriegums: katras ķīmijas nominālais voltāžas līmenis (piem., li-ion ~3,6–3,7 V, NiMH/NiCd ~1,2 V, alkalīnskābes šūna ~1,5 V, svina‑skābes šūna ~2,0 V).
- Jauda (kapacitāte): mēra ampēr‑stundās (Ah) vai miliampēr‑stundās (mAh) — cik ilgi akumulators var darbināt ierīci pie noteikta strāvas patēriņa.
- Iekšējais pretestības līmenis: ietekmē, cik labi akumulators spēj dot lielu strāvu un cik daudz sprieguma pazudums notiek pie slodzes.
- Ciklu skaits un kalpošanas laiks: cik reizes akumulators var pilnībā uzlādēties un izlādēties, pirms kapacitāte būtiski samazinās.
- Dziļums (Depth of Discharge, DoD): cik liels procents no kopējās kapacitātes tiek iztukšots — dziļa izlāde parasti samazina ciklu skaitu.
Akumulatoru veidi un to īpatnības
Akumulatorus iedala pēc to izmantošanas iespējas (primārie vs sekundārie) un pēc ķīmiskā sastāva. Biežāk sastopamie veidi:
- Svina‑skābes (Lead‑acid): lēti, noturīgi pret skarbiem apstākļiem, piemēroti automašīnām, UPS un enerģijas uzkrāšanai. Parasti zema enerģijas blīvuma, bet augsta strāvas atdeve. Svina akumulatori bieži ir ļoti labi pārstrādājami.
- NiCd (nikle‑kadmijs): izturīgi pret augstām temperatūrām un lielām slodzēm, bet satur kaitīgu kadmiju un ir pakļauti "memories" efektam.
- NiMH (nikle‑metālu hidrīds): labāka kapacitāte nekā NiCd un mazāk "memory" efekta; izmanto kombinācijās ar portatīvajiem instrumentiem un baterijām (AA, AAA).
- Alkalīnskābes primārās baterijas: vienreizējās lietošanas baterijas (AA, AAA u.c.) ar nominālo spriegumu ~1,5 V. Lētas un plaši pieejamas.
- Litija jonu (Li‑ion) un litija polimēru (Li‑Po): augsta enerģijas blīvuma, salīdzinoši vieglas — plaši lieto mobilajās ierīcēs, datoros un elektrotransportā. Prasīgas uzlādes un drošības vadībā (risks termiskai runaway, jāievēro drošas lādēšanas spriegumi un temperatūras robežas).
Uzlāde un izlāde — praktiski
- Uzlādes režīmi: Li‑ion parasti uzlādē CC‑CV (konstanta strāva, pēc tam konstants spriegums). Svina‑skābes var uzlādēt ar konstantu spriegumu vai impulsu režīmiem.
- Izlādes strāva: daudzas ierīces prasa lielu īslaicīgu strāvu (piem., starterim automašīnā), citiem svarīga ir ilga, zema strāva (piem., saules enerģijas uzkrāšana).
- Pārlādēšana un pilnīga izlāde: pārlādēšana, īpaši bez pareizas vadības, var bojāt akumulatoru (vai izraisīt ugunsgrēku); daudzi sekundārie akumulatori cieš, ja tie tiek pilnībā izlādēti (atkarīgs no ķīmijas).
- Temperatūras ietekme: zemas temperatūras samazina efektīvo jaudu, augstas temperatūras paātrina nodilumu.
Drošība un pareiza lietošana
- Izmantojiet tikai ieteicamos lādētājus un ievērojiet ražotāja norādījumus.
- Nepakļaujiet akumulatorus pārmērīgai siltumam, liesmai vai mehāniskiem bojājumiem.
- Li‑ion baterijas var aizdegties pie bojājuma vai nepareizas uzlādes — izvairieties no bedrēm, īssavienojumiem un pārslodzes.
- Primārās baterijas nedrīkst mēģināt uzlādēt, ja tās nav paredzētas uzlādei.
Vides ilgtspēja un pārstrāde
Dažas bateriju ķīmijas satur smagus metālus (piem., svins, kadmijs) un baterijas jāvāc atsevišķi un jānodod pārstrādei. Svina‑skābes akumulatori parasti tiek ļoti efektīvi pārstrādāti, savukārt litija bateriju pārstrāde attīstās, bet prasības pieaug. Pareiza utilizācija samazina vides piesārņojumu un ļauj atgūt vērtīgas izejvielas.
Pielietojumi
- Mobilās ierīces: telefoni, planšetes, klēpjdatori (galvenokārt Li‑ion).
- Transportlīdzekļi: sākot no automašīnu starteriem (svina‑skābes) līdz pilnībā elektriskiem transportlīdzekļiem (Li‑ion baterijas enerģijas pārvaldībai).
- Energijas uzkrāšana: rezerves barošanas avoti (UPS), saules enerģijas sistēmas.
- Rīki, rotaļlietas un medicīniskās ierīces.
Kā izvēlēties akumulatoru
Izvēloties akumulatoru, ņemiet vērā:
- Enerģijas blīvumu: cik daudz enerģijas vienā svara vai tilpuma vienībā.
- Jaudas prasības: vai nepieciešama liela strāva īsu laiku vai ilga darbība pie mazāka patēriņa.
- Ciklu dzīve un uzticamība: cik ilgi akumulators kalpos konkrētā pielietojumā.
- Kostu un drošība: sākotnējās izmaksas pret ekspluatācijas un apkalpošanas izmaksām.
Kopsavilkums — praktiski padomi
- Izmantojiet ražotāja ieteiktos lādētājus un neļaujiet akumulatoriem pārsilt.
- Uzglabājiet sekundāros akumulatorus vēsā, sausā vietā ar daļēju uzlādi, ja tie netiks izmantoti ilgu laiku.
- Atdodiet izlietotās baterijas pārstrādei — tas ir drošāk un videi draudzīgāk.