Osmozi sauc par ūdens (šķīdinātāja) kustību caur daļēji caurlaidīgu membrānu no reģiona ar zemāku izšķīdušo vielu koncentrāciju uz reģionu ar augstāku izšķīdušo vielu koncentrāciju, tādējādi izlīdzinot koncentrāciju atšķirības. Osmoze ir pasīvs transports — tai nav nepieciešama ārēja enerģija — un to nosaka atšķirīgs ķīmiskais potenciāls un osmotiskais spiediens abās membrānas pusēs. Osmotisko spiedienu izraisa atšķirīga izšķīdušo vielu koncentrācija, kas rada tendenci pārvietot šķīdinātāju, lai mazinātu šo atšķirību.
Osmozes princips
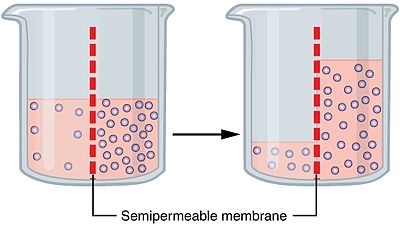
Osmoze notiek, ja pastāv daļēji caurlaidīga (semipermeabla) membrāna, kas ļauj šķīdinātājam (parasti ūdenim) šķērsot membrānu, bet neļauj viegli pārvietoties atsevišķām izšķīdušajām vielām. Ūdens plūst no puses ar lielāku brīvo šķīdinātāja daudzumu (zemāka izšķīdušo vielu koncentrācija) uz pusi ar mazāku brīvo šķīdinātāja daudzumu (augstāka izšķīdušo vielu koncentrācija). Šo plūsmu nosaka ķīmiskais potenciāls, temperatūra un šķidruma spiediens.
Osmotiskais spiediens — kvantitatīvs skaidrojums
Osmotisko spiedienu var saistīt ar izšķīdušo vielu koncentrāciju un temperatūru. Vienkāršā gadījumā to apraksta van 't Hoff likums: π = i·C·R·T, kur π ir osmotiskais spiediens, i — disociācijas koeficients, C — molārā koncentrācija, R — gāzu konstante un T — absolūtā temperatūra. Praktiski tas nozīmē, ka jo vairāk daļiņu šķīdumā, jo lielāks osmotiskais spiediens.
Osmoze šūnu membrānās
Osmoze ir īpaši nozīmīga šūnas membrānu funkcijās. Šūnas iekšiene un ārpuse var atšķirties pēc izšķīdušo vielu koncentrācijas, tādēļ ūdens pastāvīgi mēģina līdzsvarot šīs atšķirības:
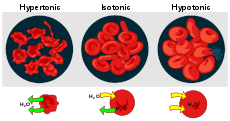
- Ja ārējā vide ir hipotoniska (mazāka izšķīdušo vielu koncentrācija nekā šūnā), ūdens ieplūdīs šūnā — tas var izraisīt šūnas piepūšanos vai plīsumu (piem., eritrocītu hemolīze).
- Ja ārējā vide ir hipertoniska (lielāka izšķīdušo vielu koncentrācija), ūdens izplūdīs no šūnas — šūna saruks un var zaudēt funkciju (piem., kruncināšanās).
- Isootoniskā vidē nosacījumi ir līdzsvaroti un netiek novērota būtiska ūdens plūsma.
Daudzas šūnas regulē savu ūdens līdzsvaru, izmantojot membrānas proteīnus — akvaporīnus — kas veicina ūdens selektīvu pārvietošanos, kā arī jonkanālus un transportierus, kas maina osmotiski aktīvo daļiņu koncentrāciju.
Toniškums un piemēri
Praktiski piemēri, kur osmoze ir svarīga:
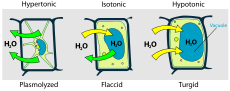
- Augi — turgors (šūnu tonuss) rodas, kad šūnas iekšienē ūdens spied uz šūnapvalku; turgora zudums noved pie vītušiem augiem.
- Dzīvnieku šūnas — hemolīze hipotoniskā šķīdumā un krēnācija hipertoniskā šķīdumā.
- Medicīnā — intravenozo šķīdumu izotoniķi jāizvēlas rūpīgi, lai nepieļautu šūnu bojāeju.
- Tehnoloģijās — reversā osmoze tiek izmantota ūdens attīrīšanā un desalinācijā.
Bioloģiskā nozīme un regulācija
Osmoze ir būtiska bioķīmijas un šūnu fizioloģijas procesiem: tā ietekmē barības vielu uzņemšanu, atkritumvielu izvadīšanu, šūnu apjomu un spiedienu. Organismi attīstījuši mehānismus osmoregulācijai — piemēram, augi izmanto vakuolas un šūnapvalku elastību, bet dzīvnieki regulē jonus caur nierēm, siltasiņu dzīvnieku osmoregulēšanu veic arī epitēlijas šūnas.
Praktiskie pielietojumi un ierobežojumi
Osmozi izmanto daudzās tehniskās un medicīniskajās jomās:
- ūdens attīrīšana un desalinācija (reversā osmoze),
- medicīniskā dialīze, kur nepieciešams atdalīt atkritumvielas no asinīm,
- pārtikas konservēšana, kur sāls vai cukura pievienošana rada hipertonisku vidi un novērš mikroorganismu augšanu.
Tomēr osmoze ir atkarīga no membrānas īpašībām — daļēji caurlaidīgas membrānas selektivitāte, poru izmērs un ķīmiskās īpašības nosaka, cik efektīvi notiek šķidruma vai atsevišķu vielu šķērsošana.
Kopumā osmoze ir fundamentāls fizikāli-ķīmisks process ar plašu nozīmi gan šūnu iekšējā līdzsvara uzturēšanā, gan daudzos praktiskos pielietojumos. Sapratne par osmozes mehānismiem palīdz skaidrot daudzus bioloģiskus fenomenu un optimizēt tehnoloģiskos risinājumus.