CRISPR ir mikrobioloģijā lietots termins. Tas apzīmē Clustered Regularly-Interspaced Short Palindromic Repeats (regulāri izkaisīti īsi palindromiski atkārtojumi). Tie ir dabisks ģenētiskā koda segments, kas sastopams prokariotos: tas ir lielākajā daļā baktēriju un arheju.
CRISPR ir daudz īsu atkārtotu sekvenču. Šīs sekvences ir daļa no prokariotu adaptīvās imūnsistēmas. Tas ļauj tiem atcerēties un pretoties citiem organismiem, kas tos plosa, piemēram, bakteriofāgiem.
Tām ir potenciāls modificēt gandrīz jebkura organisma gēnus. Tie ir daļa no rīka, kas ļauj precīzi un mērķtiecīgi griezt un ievietot gēnus ģenētiskās modifikācijas (ĢM) procesā. Pašlaik tiek strādāts pie tā, lai noskaidrotu, kā tos var izmantot vīrusu slimību apkarošanai cilvēkiem.
Kas ir CRISPR sistēma un no kā tā sastāv?
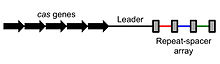
CRISPR locī ir divas galvenās sastāvdaļas:
- Atkārtojumi un spaceri — īsi palindromiski atkārtojumi, kas atdala starpsveces (spacerus). Spaceri ir īsas DNS sekvences, kas tiek iegūtas no iebrukuma avotiem (piem., fāgiem) un kalpo kā “gudrības arhīvs”, kas ļauj prokariotiem atpazīt atkārtotus uzbrukumus.
- Cas proteīni (CRISPR-associated proteins) — enzīmi, kas veic atpazīšanu un nogriešanu vai nesaudzīgu inaktivēšanu. Piemēram, Cas9 ir labi izpētīts nukleāzes tips, kas spēj veikt divkāršu DNS lūzumu mērķa vietā.
Kā CRISPR-Cas sistēma darbojas?
Darbošanās parasti sastāv no trim posmiem:
- Adaptācija (spacer iegūšana) — kad baktērija vai arheja saskaras ar ārējo DNS (piem., fāga genomu), daļa no šīs DNS var tikt integrēta CRISPR lokā kā jauns spacer.
- Ekspresija un procesēšana — CRISPR loks tiek transkribēts kā ilgāks pre-crRNA, kas tiek apstrādāts un sadalīts atsevišķos crRNA (guide RNA). Dažos sistēmas veidos nepieciešama arī tracrRNA, kas sadarbojas ar crRNA.
- Interference (uzbrukums) — crRNA kopā ar Cas proteīnu atpazīst atkārtotā iebrukuma secību un nogriež to. Daudzi Cas proteīni atpazīst mērķi tikai, ja tajā blakus ir specifiska īsa motīva, ko sauc par PAM (Protospacer Adjacent Motif).
Sistēmu veidi un rīki
Ir vairāki CRISPR-Cas sistēmu tipi (I, II, III utt.), katram no tiem ir atšķirīgas īpašības. Laboratoriskās un medicīniskās izmantošanas ziņā visplašāk izmantotie rīki ir:
- Cas9 — DNA mērķējoša kvarātāze, plaši izmantota ģenomu rediģēšanā.
- Cas12 — arī DNA mērķējošs, bet ar atšķirīgām īpašībām un diagnostikas iespējām.
- Cas13 — RNA mērķējošs enzīms, noderīgs vīrusos balstītu RNS patogēnu nosakšanai vai to inaktivēšanai.
- Tālāk attīstīti ierīki: base editors (ļauj mainīt atsevišķus nukleotīdus bez dubultās DNS lūzuma) un prime editing (prezīzāka rediģēšana ar mazāku bojājumu risku).
Pielietojumi
- Biomedicīna: monogēnu slimību terapija (piem., ārstēšanas pētījumi sirpjveida anēmijas, Lebera iedzimtā tīklenes atrofijas u.c.), onkoloģija (imūnterapijas modifikācijas) un potenciālas antivirālas stratēģijas.
- Agronomija: kultūraugu uzlabošana (rezistence pret slimībām, ražas kvalitātes uzlabošana) bez tradicionālajiem transgēniem risinājumiem.
- Diagnostika: sistēmas kā SHERLOCK (Cas13) un DETECTR (Cas12) ļauj ātri, jutīgi un lēti noteikt vīrusus un citas nukleīnskābes uz vietas.
- Pamatizpēte: gēnu funkciju noskaidrošana, ģenomu skenēšana un šūnu līniju izveide modelēšanai.
Drošība, precizitāte un ētika
CRISPR tehnoloģija ir spēcīga, bet tai ir arī ierobežojumi un riski:
- Off-target efekti — nenojauši rediģējumi citās vietās genomā var radīt nevēlamas sekas. Tāpēc izstrādā augstākas precizitātes Cas variācijas un uzlabo vadības RNA dizainu.
- Piegādes izaicinājumi — efektīva un droša rediģējošo elementu piegāde cilvēka šūnām (piem., vektori, lipīdu nanoplaiks) joprojām prasa optimizāciju.
- Imūnreakcijas risks — cilvēka imūnsistēma var atpazīt prokariotu izcelsmes Cas proteīnus kā svešķermeņus.
- Ētiskas un regulatīvas problēmas — īpaši attiecībā uz dzimumlīnijas rediģēšanu (germline editing), ekosistēmu ietekmi un piekļuves vienlīdzību ārstniecībai.
Nākotnes virzieni
Pētniecība turpinās, lai uzlabotu mērķprecizitāti, samazinātu blakusefektus, izstrādātu drošākas piegādes metodes un paplašinātu pielietojumus. Tāpat notiek darbs pie CRISPR balstītiem antivielu un antivīrusu terapeitiskiem risinājumiem, kā arī ātriem diagnostikas testiem. Nozinātniskā kopiena un sabiedrība turpina diskusijas par ētiskajiem un regulatīvajiem pamatiem, lai nodrošinātu drošu un taisnīgu tehnoloģijas izmantošanu.
CRISPR sistēma apvieno prokariotu dabisko imūnatbildi ar jaudīgiem biotehnoloģiskiem rīkiem, un tās attīstība turpmākajos gados var radikāli mainīt medicīnu, lauksaimniecību un diagnostiku — ja vien riski un ētiskie jautājumi tiks pienācīgi adresēti.