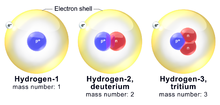
Ķīmiskā elementa atomi var pastāvēt dažādās formās — tos sauc par izotopiem. Izotopiem ir vienāds skaits protonu (un elektronu), bet atšķirīgs skaits neitronu. Tādēļ viena un tā paša elementa izotopi atšķiras pēc masas — to masas neatbilst viena otrai.
Masas skaitlis un atoma sastāvs
Masas skaitlis (parasti apzīmēts ar A) ir protonu un neitronu summa atomā. To var izteikt vienādojumā: A = Z + N, kur Z ir protonu skaits (atomnumurs), bet N ir neitronu skaits. Proti, ja zināms elementa atomnumurs un konkrētā izotopa masas skaitlis, var aprēķināt neitronu skaitu.
Atšķirībā no masas skaitļa, kas ir veselais skaitlis, atommasa (vai relatīvā atoma masa) ir vidējā vērtība, kas ņem vērā visu dabā sastopamo izotopu masas un to relatīvās abundances (sastopamības procentu). Piemēram, hloram ir divi galvenie izotopi 35Cl un 37Cl, un to relatīvā sastopamība nosaka hloru raksturojošo relatīvo atommasu.
Atoma elektroni un ķīmiskās īpašības
Neitrālā atomā elektronu skaits parasti sakrīt ar protonu skaitu. Tāpēc viena elementa izotopiem ir vienāda elektroniskā struktūra. Tā kā ķīmiskās reakcijas galvenokārt nosaka elektronu izvietojums, izotopi ķīmiski parasti izturas ļoti līdzīgi. Tomēr fiziskās īpašības, piemēram, masa un blīvums, var būt atšķirīgas.
Masas efekts un reakciju ātrums
Smagākiem izotopiem ķīmiskās reakcijas dažkārt norit lēnāk — šo parādību sauc par masas efektu vai kinetisko izotopu efektu. Tas ir izteiktāks viegliem elementiem; labi zināms piemērs ir ūdens izotopi:
- protijam (1H) — visvieglākais ūdeņraža izotops;
- deitērijam (2H) — masa aptuveni divreiz lielāka nekā procijam;
- tritijs (3H) — radioaktīvs, smagāks ūdeņraža izotops.
Vieglākiem elementiem masas attiecība starp izotopiem ir liela, tāpēc masas efekts ir pamanāmāks. Smagākiem elementiem relatīvā atommasu atšķirība parasti ir neliela, un ķīmiskā uzvedība praktiski nesakrīt.
Stabilie un radioaktīvie izotopi
Daži izotopi ir stabili — tie nemainās kodolā laika gaitā. Citi ir radioaktīvi (nestabili) un pašsabrūk, izstaro radiāciju un pārvēršas par citiem elementiem vai to izotopiem. Radioaktivitātei raksturīgs jēdziens — pusi noejas laiks (pusperiods), kas norāda laiku, pēc kura puse no sākotnējā daudzuma ir sabrukusi.
Praktiska nozīme un pielietojumi
Izotopiem ir daudz praktisku pielietojumu:
- arheoloģijā un ģeoloģijā: radiokarbona datēšana (14C) nosaka organisku materiālu vecumu;
- medicīnā: diagnostikā un terapijā izmanto radioaktīvos izotopus (piem., PET skenēšanai, radioķīmijai);
- pētījumi: izotopu marķieri (traceri) ļauj izsekot ķīmiskos ceļus un bioloģiskās vielmaiņas procesus;
- enerģētikā: kodolenerģijas ražošanā izmanto urāna un plutonija izotopus;
- rūpniecībā un zinātnē: izotopu attīrīšana, analīze un materiālu izpēte.
Vēl daži svarīgi jēdzieni
Izotopu sastopamība — procentuālā daļa, kādā konkrēts izotops sastopams dabā vai paraugā. Izotopiskā frakcionēšana — procesi, kas maina izotopu attiecību (piem., ķīmiskās vai fizikālās izdalīšanās laikā). Vidējā atommasa tiek aprēķināta, ņemot vērā visu izotopu masas un to relatīvās abundances.
Apkopojot: izotopi ir viena elementa atomu varianti ar vienādu protonu, bet atšķirīgu neitronu skaitu. Tas nosaka to masas skaitli, ietekmē fizikālās īpašības un dažkārt arī reakciju kinetiku, tomēr ķīmiskās īpašības lielākoties saglabājas līdzīgas.