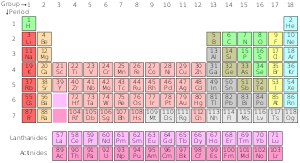
Ķīmisko elementu periodiskā tabula ir zināmo ķīmisko elementu saraksts. Tabulā elementi ir sakārtoti to atomu numuru secībā, sākot ar mazāko atomu skaitu - ūdeņradi. Elementa atomu skaits ir vienāds ar protonu skaitu konkrētajā atoma kodolā. Periodiskajā tabulā elementi ir sakārtoti periodos un grupās. Elementu rindu tabulā sauc par periodu. Katram periodam ir numurs; no 1 līdz 8. Pirmajā periodā ir tikai divi elementi: ūdeņradis un hēlijs. Gan 2. periodā, gan 3. periodā ir 8 elementi. Citi periodi ir garāki. Elementiem periodā ir secīgi atomnumu numuri.
Elementu kolonnu, kas atrodas tabulā, sauc par grupu. Standarta periodiskajā tabulā ir 18 grupas. Katrai grupai ir numurs: no 1 līdz 18. Elementiem grupā ir līdzīgi izkārtoti elektroni, atkarībā no valences elektronu skaita, kas tiem piešķir līdzīgas ķīmiskās īpašības (tie uzvedas līdzīgi). Piemēram, 18. grupu sauc par cēlgāzēm, jo tās visas ir gāzes un nesavienojas ar citiem atomiem.
Pastāv divas grupu numuru sistēmas; vienā tiek izmantoti arābu cipari (1,2,3), bet otrā - romiešu cipari (I, II, III). Romas skaitļu nosaukumi tika lietoti lielāko daļu 20. gadsimta. Starptautiskā teorētiskās un lietišķās ķīmijas savienība (IUPAC) 1990. gadā nolēma izmantot jauno sistēmu ar arābu cipariem, lai aizstātu divas vecās grupu sistēmas, kurās izmantoja romiešu ciparus.
Ķīmiķi ir izmantojuši periodisko tabulu, lai novērotu likumsakarības un sakarības starp elementiem. Periodiskajā tabulā ir trīs galvenās grupas: metāli, metaloīdi un nemetāli. Piemēram, elementi tabulas lejasdaļā un galēji kreisajā pusē ir vismetāliskākie, bet elementi augšējā labajā pusē ir vismazāk metāliski. (piemēram, cēzijs ir daudz metāliskāks par hēliju). Pastāv arī daudzas otras likumsakarības un attiecības.
Periodisko tabulu izgudroja krievu ķīmiķis Dmitrijs IvanovičsMendeļejevs (1834-1907). Viņam par godu tika nosaukts 101. elements - mendeļejevs.
Kas nosaka elementu vietu tabulā
Galvenais princips ir periodiskais likums: elementu īpašības mainās periodiski, kad tie tiek sakārtoti pēc augoša atomnumura. Atomnumurs (protonu skaits) nosaka elementa ķīmisko dabu, bet elektronu izvietojums (elektronkonfigurācija) nosaka, kā elements savienojas ar citiem un kādas īpašības tam piemīt. Īpaši svarīgi ir ārējie (valences) elektroni, jo tie nosaka ķīmiskās reakcijas un grupas līdzību.
Tabulas daļas un bloki
- s‑bloks — grupas 1–2 (un hēlijs). Šajos elementiem ārējie elektroni atrodas s‑orbitalē.
- p‑bloks — grupas 13–18. Šeit valences elektroni p‑orbitalēs; p‑bloks satur gan nemetālus, gan metālus un cēlgāzes.
- d‑bloks (pārejas metāli) — grupas 3–12; raksturīgas d‑elektronu izmantošana ķīmiskajās īpašībās un dažādas oksidācijas pakāpes.
- f‑bloks — lantanoīdi (lanthanides) un aktinoīdi (actinides), parasti novietoti atsevišķā rindā zem galvenās tabulas. Tie ietver reti sastopamos un radioaktīvos elementus.
Grupu piemēri un nosaukumi
Dažas grupas ir īpaši nosauktas un viegli atpazīstamas pēc īpašībām:
- 1. grupa — alkālmetāli (nātrijs, kālijs utt.). Spēcīgi metāli, reaģē ar ūdeni.
- 2. grupa — sārmainie zemes metāli (magnijs, kalcijs). Mazāk reaktīvi nekā 1. grupas elementi.
- 17. grupa — halogēni (fluors, hloru u.c.). Ļoti reaģējoši nemetāli.
- 18. grupa — cēlgāzes (inertās gāzes), kas lielākoties ir ķīmiski neaktīvas.
- Pārejas metāli (d‑bloks) — bieži katalizē reakcijas, veido krāsainus savienojumus un vairākas oksidācijas pakāpes.
Galvenās periodiskās tendences
- Atomradio — palielinās, ejot uz leju grupā; samazinās, ejot no kreisās uz labo periodā (efektīva kodola lādiņa pieaugums).
- Jonizācijas enerģija — enerģija, kas nepieciešama, lai noņemtu elektronu; palielinās uz augšu un pa labi tabulā.
- Elektronegatīvība — spēja piesaistīt kopīgus elektronus; palielinās uz augšu un pa labi (izņemot cēlgāzes).
- Metāliskums — metāliskas īpašības pieaug, ejot uz leju un pa kreisi.
Lantanoīdi un aktinoīdi
Lantanoīdi (½ periodā pēc lantāna) un aktinoīdi (aktīnijam sekojošā rinda) bieži tiek parādīti atsevišķi tabulas apakšā, lai saglabātu galveno tabulas formu. Lielākā daļa aktinoīdu ir radioaktīvi un daudzi ir mākslīgi radīti. Šie elementi bieži izmanto specializētās tehnoloģijās, piemēram, magnētos, kodoldegvielā un radioterapijā.
Praktiska nozīme un lietojumi
Periodiskā tabula nav tikai teorētisks rīks — tā palīdz prognozēt vielu īpašības, izvēlēties elementus rūpniecībā, materiālzinātnē un medicīnā. Piemēram, metālu izvēle konstrukcijām, pusvadītāju materiāli (silīcijs p‑blokā), vai magnētiskie materiāli (daži lantanoīdi) balstās uz to vietu tabulā un elektronkonfigurāciju.
Vēsture un prognozes
Periodiskās tabulas saknes meklējamas 19. gadsimtā. Tieši Dmitrijs IvanovičsMendeļejevs sakārtoja elementus pēc to īpašībām un atommasām (vēl pirms atomnumura precīzas izpratnes) un veiksmīgi prognozēja vairākus tad vēl nezināmus elementus, atstājot tukšas vietas tabulā. Vēlāk, nosakot atomnumurus, tabula tika pielāgota mūsdienu formā.
Modernie papildinājumi
Mūsdienās zināmi 118 elementi (līdz 118. elementam, oganesson). Daudzi augsta atomnumura elementi ir mākslīgi radīti laboratorijās un ir ļoti īslaicīgi; tie tiek iekļauti tabulā pēc to atklāšanas un apstiprināšanas. IUPAC nosaka grupu numerāciju un elementu nosaukumus, lai nodrošinātu vienotu sistēmu visā pasaulē.
Kā lasīt tabulu īsi
- Skaties uz periodu (rinda) — tas norāda, cik elektronapvalku elementam ir.
- Skaties uz grupu (kolonna) — sniedz informāciju par valences elektroniem un līdzīgām ķīmiskajām īpašībām elementiem tajā pašā kolonnā.
- Atceries blokus (s, p, d, f) — tie palīdz saprast, kur atrodas valences elektroni un kādas īpašības sagaidāmas.
Periodiskā tabula ir dinamisks rīks: tā tiek uzlabota un precizēta, kad atklāj jaunas īpašības vai jaunus elementus, tomēr tās pamatprincipi — atomnumurs, elektronkonfigurācija un periodiskie modeļi — paliek nemainīgi un turpina būt pamats ķīmijas izpratnei.