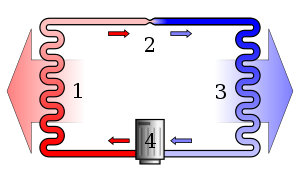
Otrais termodinamikas likums nosaka, ka, mainoties enerģijai no vienas formas uz citu vai matērijai brīvi pārvietojoties, entropija (nekārtība) slēgtā sistēmā parasti palielinās. Tas ir pamatprincips, kas nosaka ne tikai siltuma un darba apmaiņu, bet arī procesa virzienu — kuru pāreju termodinamikā var saukt par "spontānu" un kuru ne.
Svarīgi precizēt, ko nozīmē «slēgta sistēma» un «entropijas palielināšanās»: parasti runājam par izolētu (neapmainīgu ar enerģiju un matēriju) sistēmu — tās entropija laika gaitā nepalielinās mazāk bieži; makroskopiskām sistēmām entropijas pieaugums ir praktiski noteikts, bet mikroskopiskām sistēmām iespējamas novērojamas svārstības (termiskie svārstījumi).
Entropijas jēdziens un skaidrojums
Entropija ir rādītājs tam, cik daudz veidos enerģija vai matērija var izplatīties sistēmā. No statistiskās fizikas skatu punkta entropija ir saistīta ar iespējamām mikrostāvokļu skaitām — Bolcmaņa formulā:
S = k ln W,
kur S ir entropija, k — Bolcmaņa konstante, W — iespējamo mikrostāvokļu skaits, kas atbilst dotajam makrostāvoklim. Jo vairāk mikrostāvokļu, jo lielāka entropija.
Termodinamikā entropijas maiņu pie temperatūras T reversā procesā raksturo izteiksme dS = δQ_rev / T. Parasti vēlamies atzīmēt, ka reālos (ne-reversālos) procesos entropija pieaug — matemātiski dS > δQ / T.
Vispārīgākie formulējumi
Otrā likuma formulējumi var tikt izteikti dažādiem vārdiem, taču visi tie savieno vienu un to pašu domu par procesa virzienu.
Visizplatītākais termodinamikas otrā likuma formulējums ir saistīts ar Rūdolfu Klauziju:
Siltums pats no sevis nevar pāriet no aukstākas uz karstāku ķermeni.
Tas nozīmē, ka, ja diviem ķermeņiem ir dažādas temperatūras, siltums spontāni plūs tikai no karstākā uz aukstāko; lai siltums kustētos pretējā virzienā (no aukstā uz karstāku), nepieciešams veikt darbu.
Lorda Kelvina izteiktais formulējums uzsver enerģijas pārvēršanas ierobežojumus:
Pārveidošana, kuras vienīgais galarezultāts ir siltuma, kas iegūts no avota nemainīgā temperatūrā, pārvēršana darbā, nav iespējama.
Praktiski tas nozīmē: nav iespējams izveidot ideālu siltummotora ciklu, kas pilnībā pārvērš visu uzņemto siltumu darbā bez jebkādām zudumiem vai siltuma noplūdēm. Reāli motori vienmēr zaudē daļu enerģijas kā siltumu.
Vēl viens — statistisks — formulējums: otrais likums ir probabilistisks likums. Ja sistēma ir pietiekami liela (daudz daļiņu), tad stāvokļi ar lielāku entropiju (vairāk mikrostāvokļu) dominē, un sistēma gandrīz noteikti pāries uz šiem stāvokļiem. Tomēr mikroskopiskā mērogā var novērot pagaidu izņēmumus (fluktuācijas).
Piemēri un ilustrācijas
- Siltumu plūsma starp ķermeņiem: ja karstais metāla gabals tiek ievietots aukstā ūdenī, siltums plūst no metāla uz ūdeni līdz temperatūras izlīdzināšanai — entropija kopumā palielinās.
- Ledus kūšana: siltuma uzsūkšanās ledum palielina ūdens molekulu iespējamo mikrostāvokļu skaitu — entropija pieaug.
- Gāzu sajaukšanās: divu atdalītu gāzu maisījums (bez jēdzieniska darba) palielina entropiju, jo daļiņām pieaug pieejamo izvietojuma stāvokļu skaits.
- Siltummotori un dzesētāji: ideāla, 100% efektīva pārveide no siltuma uz darbu ir neiespējama (Kelvina princips); dzesētājii (refrigeratori) var pārvietot siltumu no auksta uz karstu objektu tikai, ja tiek patērēts darbs.
- Brīvas ekspansijas piemērs: ideālā gāze, kas brīvi izplešas vakuumā, neatgriezeniski izplešas un entropija palielinās, jo palielinās iespējamo mikrostāvokļu skaits.
Izņēmumi, ierobežojumi un mūsdienu papildinājumi
Otrais likums nav absolūts noteikums mikroskopiskā līmenī — maziem skaitļiem daļiņu iespējamās fluktuācijas var uz īsu brīdi dot pretēju efektu. Mūsdienu teorijas, piemēram, svārstību teorija (fluctuation theorems), precizē statistisko dabu otrajam likumam un apraksta varbūtības, ar kādām var rasties entropijas samazināšanās īslaicīgās situācijās.
Terminu «entropija» izmanto arī informācijas teorijā (Šenona entropija), kur tā apraksta neziņu vai informācijas daudzumu; šie jēdzieni ir tuvi, taču nav identiski fiziskajai entropijai bez papildu interpretācijām.
Kopsavilkums
Otrais termodinamikas likums nosaka procesu virzienu termodinamikā: izolētā sistēmā entropija laika gaitā parasti palielinās, un procesi, kas samazina entropiju, prasa darbību vai ir ārkārtīgi reti mikroskopiskā līmenī. Formulējumos, ko devis Klauzijs un Kelvins, izpaužas divas pretstatāmas, bet ekvivalentas idejas: siltums nevar spontāni plūst no aukstākas vietas uz karstāku, un nav iespējams pilnībā pārvērst siltumu darbā bez zudumiem. Šie principi nosaka ierobežojumus daudzām tehnoloģijām — no siltummotoriem līdz dzesēšanas iekārtām — un ir pamats plašai termodinamikas un statistikas fizikas teorijai.
Otrais likums vispilnīgāk darbojas makroskopiskās (lielās) sistēmās; praktiski runājot, jo lielāka sistēma, jo drošāk tas jāuztver kā likums, bet mikroskopiskajā mērogā jāņem vērā arī varbūtību un fluktuāciju likumi.