Pastāv vairāki oglekļa alotropi. Pazīstamākie no tiem ir dimants un grafīts. Grafīts ir pusvadītājs, pusmetāls (elements, kas daļēji ir metāls un nemetāls, piemēram, melnais fosfors un pelēkais selēns). To var izmantot, piemēram, kā materiālu elektriskā loka lampas elektrodos. Grafīts ir visstabilākā cietā oglekļa forma, kāda jebkad atklāta.
Alotropi ir viena un tā paša ķīmiskā elementa dažādas formas. Visi elementi ir unikāli veidoti no saviem atomiem. Jebkuras fizikālās atšķirības ir saistītas ar to, kā atomi ir savienoti kopā. Daudziem elementiem piemīt alotropija, jo ir vairāki veidi, kā atomi var tikt savienoti kopā. Tāpat ir dažādi veidi, kā molekulas var sakārtot, lai veidotu lielākas struktūras.
Atšķirības atomu saistībās: sp3, sp2 un sp
Ogleklim daudzveidība rodas galvenokārt no tā, kā oglekļa atomi savieno savus četrus valentuma elektronus. Galvenie hibridizācijas veidi ir:
- sp3: katrs oglekļa atoms ir saistīts ar četriem citiem atomiem tetraedriskā konfigurācijā — tāds saistījums veido dimantu. sp3 saišu dēļ dimens ir ārkārtīgi ciets un izolē elektrību.
- sp2: trīs kovalentās saites vienā plaknē un viena brīvā p-saita veido slāņveida struktūru — to redzam grafītā un grafēnā. sp2 saites nodrošina labu elektrisko vadītspēju plaknēs un lielu mehānisko izturību dažos virzienos.
- sp: lineārs saistījums, retāk sastopams alotrops (piemēram, karbīns), ar atšķirīgām fizikālām īpašībām.
Dimants — īpašības un pielietojums
Dimants ir viens no pazīstamākajiem oglekļa alotropiem. Tā cietība un augstā gaismas izkliedēšana padara to piemērotu izmantošanai juvelierizstrādājumos. To izmanto arī rūpniecībā. Dimants ir cietākais zināmais dabiskais minerāls. Tāpēc tas ir lielisks abrazīvs. Dimants arī labi saglabā savu spīdumu. Gan dimantam, gan grafītam ir ārkārtēji augsta kušanas temperatūra, kas ir neparasta nemetāliskiem elementiem.
Papildu fakti par dimantu:
- Struktūra: atomi saistīti ar sp3 hibridizāciju, veidojot stingru trīsdimensionālu režģi.
- Optiskās īpašības: ļoti augsts laušanās koeficients un lielisks izkliedes indekss rada spožu dzirksti juvelierizstrādājumos.
- Termiskā vadītspēja: viens no labākajiem siltuma vadītājiem starp dabīgiem materiāliem.
- Pielietojums: juvelierizstrādājumi, griešanas un slīpēšanas instrumenti, optiskie elementi, augstas veiktspējas termiskās vadīšanas komponenti un pētījumi cietvielu fizikā.
- Sintētiskie dimanti tiek ražoti ar augsta spiediena augstas temperatūras (HPHT) vai ķīmiskās tvaiku nogulsnēšanas (CVD) metodēm.
Grafīts un citi slāņveida oglekļa alotropi
Grafīts sastāv no paralēlām grafēna slāņu plaknēm, kur atomi ir saistīti ar sp2 hibridizāciju. Starp slāņiem darbojas vājas Van der Waalsas spējas, tāpēc slāņi viegli var slīdēt viens pāri otram — tas padara grafītu par labu eļļojošu materiālu un izmanto to kā saķeri (smērvielu).
- Elektriskā vadītspēja: grafīts vada elektrību labi plaknēs, tāpēc to izmanto elektrodos un elektrotehnikā.
- Termiskā stabilitāte: grafīts ir termodinamiski visstabilākā cietā oglekļa forma istabas temperatūrā un spiedienā.
- Praktiskie pielietojumi: elektrodi, smērvielas, bateriju anodi (piem., litija jonu baterijās), siltuma izkliedes materiāli un kompozīti.
Citi oglekļa alotropi — grafēns, fullerēni, oglekļa nanocaurules, amorfs ogleklis
Ogleklim ir vairākas modernas un tehnoloģiski svarīgas alotropiskas formas:
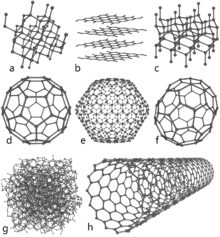
- Grafēns — viens grafīta slānis, vienu atomu biezs. Izceļas ar izcilu elektrisko vadītspēju, milzīgu mehānisko izturību un caurspīdīgumu. Grafēns sola revolucionāras iespējas elektronikā, sensoros un kompozītmateriālos.
- Fullerēni (piem., C60) — slēgtas lodes formas molekulas ar specifiskām ķīmiskām un fizikālām īpašībām; izmanto nanotehnoloģijā un pētījumos par vielu uzvedību skaitāmā mērogā.
- Oglekļa nanocaurules — cilindriskas struktūras, kas veidojas no grafēna rullīšiem; tām ir ārkārtīga stiprība, vieglums un atšķirīga elektriskā vadītspēja atkarībā no ģeometrijas.
- Amorfs ogleklis — dūņas, sērs, aktivētais ogleklis un sods; svarīgi materiāli filtrēšanā, adsorbcijā un kā katalizatoru atbalsts.
Termodinamiski un ķīmiski aspekti
Gan dimants, gan grafīts iztur ļoti augstas temperatūras un ogleklim piemērojami apstākļi, tomēr oglekļa "kušanas" uzvedība ir specifiska: pie atmosfēriskā spiediena ogleklis parasti sublimē (tieši pāriet no cietas uz gāzes fāzi) pie temperatūrām virs ~3500 °C. Grafīts parasti ir termodinamiski stabilāks par dimantu pie normāla spiediena — dimants nepieciešamības gadījumā pārvēršas grafītā (šī transformācija prasa laiku un var paātrināties pie augstas temperatūras).
Īss salīdzinājums
- Cietība: dimants >> grafīts
- Elektriskā vadītspēja: grafīts (labi plaknēs) > dimants (izolators); izņēmums — dopēts vai speciāli apstrādāts dimants var vadīt)
- Termiskā vadītspēja: dimants ļoti augsta; grafīts labā vadītspēja plaknēs
- Optika: dimants caurspīdīgs un spīdīgs; grafīts tumšs un necaurspīdīgs
Praktiski pielietojumi un nākotnes perspektīvas
Oglekļa alotropi ir plaši izmantojami gan tradicionālās nozarēs (juvelierizstrādājumi, abrazīvi, elektrodi, smērvielas), gan augsto tehnoloģiju lietojumos (baterijas, kompozītmateriāli, elektronika, nanotehnoloģijas). Īpaši grafēns un oglekļa nanostruktūras piedāvā jaunas iespējas enerģijas saglabāšanā, ātrdarbīgā elektronikā un daudzās citās jomās.
Kopumā ogleklis demonstrē, cik dažādas un funkcionāli atšķirīgas var būt viena elementa alotropiskās formas — no briljanta dimanta līdz plaukstošam grafēna nanomateriālam.