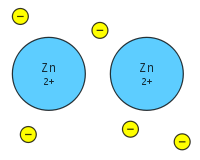
Metāliska saite ir saite, kurā daudzu atdalītu elektronu koplietošana notiek starp daudziem pozitīviem joniem, — valences elektroni delokalizējas un darbojas kā "līme", kas piešķir vielai noteiktu struktūru un kohēziju. Atšķirībā no kovalentajām vai jonu saitēm, metāliskā saite raksturojas ar to, ka valences elektroni nav stipri piesaistīti atsevišķiem atomiem, bet brīvi pārvietojas pa visu metāla kristālu, veidojot tā saukto elektronu "jūru". Metāliem parasti ir zema jonizācijas enerģija, tāpēc šo elektronus viegli delokalizēt un pārnest caur materiālu.
Elektronu "jūra" un teorētiskie modeļi
Metāliskās saites izskaidrošana bieži balstās uz elektronu jūras modeli: delokalizētie elektroni neiederas konkrētā metāla kodolā, bet brīvi pārvietojas pa kristālisko režģi, radot homogēnu negatīvu lādiņu, kas pievelk pozitīvos metāla jonus. Šā modeļa papildinājumam tiek lietota arī kvantu mehānikai balstīta joslu teorija, kas apraksta, kā atsevišķu atoma orbitāļu pārklāšanās rada enerģijas joslas (vadītspējas joslu, valences joslu u. c.) un nosaka metāla elektriskās un optiskās īpašības.
Metāliskās saites ietekmētās īpašības
Starp metāla brīvajiem elektroniem un pozitīvajiem joniem pastāv spēcīgs pievilkšanas spēks, tāpēc daudzi metāli izceļas ar šādām īpašībām:
- Augsts kušanas un vārīšanās punkts — spēcīga piesaiste starp joniem un elektronjūru prasa daudz enerģijas, lai izjauktu saites.
- Elektriskā vadītspēja — tā kā elektroni ir delokalizēti, metāli labi vada elektrību; elektrisko strāvu nodrošina šo brīvo lādiņu pārvietošanās.
- Siltuma vadītspēja — brīvie elektroni efektīvi pārnes enerģiju, padarot metālus labus siltuma vadītājus.
- Spīdums (metalisks spīdums) — brīvie elektroni absorbē un atkārtoti izstaro elektromagnētisko starojumu, radot raksturīgo spīdumu.
- Kaļamība un plastiskums — metāla atomi var pārbīdīties viens attiecībā pret otru, neizjaucot saites, jo elektronjūra saglabā kohēziju; tas nodrošina kaļamību un vilkšanas spējas.
- Izturība un blīvums — metāliskā saite nosaka arī materiāla mehāniskās īpašības, piemēram, stiprību un blīvumu, kas atkarīgs no atomu starpsaistes un elektroniskā pārklājuma.
Kristālisks režģis un koordinācijas skaitļi
Metāli parasti kristalizējas vienkāršās, cieši piepildītās struktūrās, piemēram, fcc (face-centered cubic), bcc (body-centered cubic) vai hcp (hexagonal close-packed) režģos. Šo režģu atšķirības ietekmē mehāniskās īpašības, blīvumu un termisko uzvedību. Metālu atomiem bieži ir augsti koordinācijas skaitļi (6, 8 vai 12), kas norāda uz ciešu atomu sakopojumu un stiprām metāliskajām saitēm.
Elektriskā vadītspēja, temperatūras ietekme un supravadītspēja
Tā kā elektroni brīvi pārvietojas, metālam ir zināma elektrovadītspēja, kas ļauj radīt elektrisko strāvu. Vadītspēja parasti samazinās, palielinoties temperatūrai, jo elektronus vairāk izkliedē fononu (atomu vibrāciju) ietekme, kas palielina pretestību. Tomēr daži materiāli pie zemiem temperatūras režīmiem pāriet supravadītspējā — stāvoklī, kurā pretestība pazūd pilnībā; tas ir kvantu parādības piemērs, kas saistīts ar elektronu pāru (Kupera pāru) veidošanos.
Enerģētiskie aspekti un saites stiprums
Metāliskās saites stiprums un kohēzijas enerģija ir atkarīga no valences elektronu skaita, atomu izmēra un metaisma atomu elektroniskās struktūras. Pēc ķīmiskajiem kritērijiem metāliem parasti ir vismaz viens valences elektrons, kas nav lokāli piesaistīts blakus esošajiem atomiem; to ārējās atomu orbitāles var pārklāties, veidojot plašas enerģijas joslas.
Izņēmumi un īpaši gadījumi
Ne visi metālu savienojumi un stāvokļi uzvedas vienādi. Piemēram, ir metāli un metālu joni, kas rada citus saišu tipus. Dzīvsudraba gadījumā daži joni ( Hg2+
2) ) veido kovalentās metāla–metāla saites, nevis klasisku delokalizēto elektronjūru. Tāpat pastāv nemetāli, kas vada elektrību, piemēram, grafīts (jo tam, tāpat kā metāliem, ir brīvi elektroni), kā arī jonu savienojumi, kas vada strāvu, ja tie ir izkusuši vai izšķīdināti ūdenī — šādos gadījumos lādiņu pārnēsā brīvi kustīgi joni.
Sakausējumi
Sakausējums ir metālu "šķīdums" — materiāls, kurā divi vai vairāk metālu (vai metālu ar nemetāliem) ir sajaukti vienā kristāliskā vai amorfā fāzē. Sakausējumi bieži izrāda uzlabotas īpašības salīdzinājumā ar tīriem metāliem, piemēram, paaugstinātu stiprību, izturību pret koroziju vai mainītu elektrisko vadītspēju. Lielākā daļa sakausējumu saglabā metālisku spīdumu, taču to fizikālās un mehāniskās īpašības var ļoti atšķirties atkarībā no sastāva un ražošanas tehnoloģijas.
Pielietojums un praktiskā nozīme
Metāliskā saite padara metālus par neaizvietojamiem materiāliem inženierijā, elektrotehnikā, būvniecībā un rūpniecībā — no vadiem un kontaktu materiāliem līdz strukturālām detaļām un siltummainiem. Sapratne par metālisko saišu dabu palīdz optimizēt sakausējumu sastāvus, termiskās apstrādes procesus un materialu izvēli dažādiem pielietojumiem.
Īsumā: metāliskā saite — tas ir delokalizētu valences elektronu un pozitīvo jonu savstarpējās mijiedarbības rezultāts, kas nosaka metālu raksturīgās īpašības: vadītspēju, siltumvadītspēju, spīdumu, kaļamību un daudzus citus materiālus parametrus.