Kovalentās saites ir ķīmiskās saites starp diviem nemetāla atomiem. Tās veidojas, kad atomi savstarpēji dalās ar valences elektroniem, radot kopīgas elektronu orbitāles (molekulāras orbitāles), kurās elektronblīvums ir saistīts ar abiem kodoliem. Kovalentā saite var būt vienkārša (viena kopīga elektronu pāris), dubulta (divi pāri) vai trīskārša (trīs pāri). Single (σ) saites rodas no orbitāļu pārklāšanās gar atomu kodolu virzienu, bet pi (π) saites rodas no paralēlas p-orbitāļu pārklāšanās un parasti papildina dubultās un trīskāršās saitēs. Kovalentām saitēm raksturīgs salīdzinoši liels enerģijas patēriņš, lai saiti pārraut (saistes enerģija), un noteikts saites garums, pie kura sistēma atrodas zemākajā enerģijas stāvoklī.
Elektronu slāņi, valences elektroni un orbitāles
Pilnam ārējam apvalkam parasti ir astoņi elektroni (okteta princips), izņemot gadījumus kā ūdeņradim vai hēlijam, kam pilnam pirmajam apvalkam pietiek ar diviem elektroniem. Valences elektroni ir elektroni, kas atoma ārējā apvalkā atrodas salīdzinoši brīvi un piedalās ķīmiskajās reakcijās. Elektronu čaulu struktūru nosaka kvantu mehānika, un šajā kontekstā jēdziens "orbitāle" apzīmē nevis precīzu ceļu, bet varbūtības sadalījumu, kurā elektrons visdrīzāk atradīsies.
Elektronu skaitu atomā nosaka pēc protonu skaita atomā. Elektroni riņķo ap atomu kodoliem kā kvantu mehānikā aprakstītas orbitales; pirmajā slānī ir līdz diviem elektroniem, nākamajos slāņos parasti var būt vairāk (bieži līdz astoņiem valences elektroniem). Atomu spējas veidot kovalentas saites un saites skaits parasti ir atkarīgs no to valences elektronu skaita un orbitalu konfigurācijas.
Saites veidošanās — orbitalu pārklāšanās un enerģija
Kovalentās saites veidojas, kad atoma orbitales pārklājas, radot molekulāras orbitales ar zemāku kopējo enerģiju nekā atsevišķo atomu orbitales. Šādas pārklāšanās rezultātā elektronblīvums starp kodoliem palielinās, un tas rada piesaisti starp kodoliem un kopējo elektronu blīvumu — stabilizējošs efekts, kas notiek, līdz tiek sasniegta zemāka enerģijas stāvokļa konfigurācija. Dažkārt saites veidošanās laikā tiek atbrīvota enerģija, kas var izstaroties kā siltums vai, retāk, kā fotonu.
Svarīgi: kovalentā saite nozīmē elektronu dalīšanos, nevis pilnīgu elektrona pārnešanu (kā jonu saitēs). Ja dalīšanās ir pilnīgi vienāda (piem., H−H vai Cl−Cl), saite ir nepolāra kovalenta. Ja dalīšanās ir nevienlīdzīga, jo viens atoms ir spēcīgāks elektronu pievilcējs (augstāka elektronegatīvā vērtība), elektronblīvums nokrīt tuvāk šim atomam, veidojot daļēju negatīvu lādiņu uz tā un daļēju pozitīvu lādiņu uz otra atoma — tā rodas polāra kovalentā saite.
Polaritāte un piemēri
Polaritāti nosaka atoma elektronegatīvums un molekulas ģeometrija. Pat ja atsevišķas saites molekulā ir polāras, to dipoli var savstarpēji kompensēt atkarībā no molekulas formas (piemēram, lineārais CO2 ir nepolārs, jo dipoli pretēji viens otram atceļas). Savukārt asymetriski veidotas molekulas ar polārām saitēm parasti ir polāras kopumā.
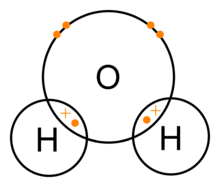
Konkrēts piemērs — ūdens, molekulā H2O: ūdeņradis (H) un skābeklis (O) saistās ar divām kovalentām saitēm. Skābeklis ir daudz elektronegatīvāks par ūdeņradi, tāpēc elektronblīvums nedaudz pārvietojas tuvāk skābeklim, padarot skābekli daļēji negatīvu, bet ūdeņraža atomus daļēji pozitīvus. Turklāt ūdens molekula ir saliekta (leņķis apm. 104,5°) sakarā ar skābekļa divām vientuļajām elektronpāru orbitalēm, un šī ģeometrija novērš dipolu kompensāciju. Rezultātā ūdens ir polāra molekula, kas ļauj veidoties ūdeņraža saitēm starp molekulām — tas dod ūdenim raksturīgās īpašības: augstu viršanas temperatūru, labu šķīdību polāros savienojumos un augstu specifisko siltumu.
Vēl daži piemēri:
- H2 — divu ūdeņraža atomu vienkārša kovalentā saite, nepolāra.
- HCl — polāra kovalentā saite, jo hloram ir lielāka elektronegatīvā spēja nekā ūdeņradim.
- CH4 (metāns) — četras vienkāršas kovalentās saites; molekula ir simetrisks tetraēdrs un nepolāra kopumā.
- Dimanta kristālrežģis — tīri kovalentā, bet ne-molekulārā tīklojuma struktūra, kur katrs oglekļa atoms veido četras spēcīgas σ saites; tā rada ļoti cietu materiālu.
Ir arī koordinētās (datora) kovalentās saites, kurā abi kopīgie elektroni sākotnēji nāk no viena atoma (donora) un otra atoms darbojas kā akceptors; tomēr rezultāts parasti tiek uzskatīts par kovalentu, jo elektroni tiek kopīgi izmantoti.
Kopumā kovalentās saites ir pamats molekulārās ķīmijas, nosakot molekulu formu, ķīmisko reaktivitāti, fizikālās īpašības un mijiedarbību starp vielām. Izpratne par orbitalu pārklāšanos, elektronegatīvumu un molekulas ģeometriju palīdz paredzēt, vai saite būs spēcīga, vai molekula būs polāra vai nepolāra, kā arī tās fizikālās īpašības.