Elektronu apvalks ir atoma ārējā daļa ap atoma kodolu. Tajā atrodas elektroni, un tā ir atoma orbitāļu grupa ar vienādu galvenā kvantu n skaitļa vērtību. Katram apvalkam piemīt noteikta enerģija un pamata attālums no kodola — apvalku numerācija sākas ar n=1 (tuvākais kodolam) un turpinās uz āru: n=2, 3, 4 utt.
Čaulu un apakščaulu struktūra
Katrai elektronārajai čaulai var būt viena vai vairākas elektronu apakščaulas jeb apakšlīmeņi, kuri atbilst dažādām orbitāļu grupām. Apakšlīmeņu veidi atkarīgi no leņķiskā momenta kvantu skaitļa l:
- s (l = 0) — viena orbitāle, maksimāli 2 elektroni;
- p (l = 1) — trīs orbitāles, maksimāli 6 elektroni;
- d (l = 2) — piecas orbitāles, maksimāli 10 elektroni;
- f (l = 3) — septiņas orbitāles, maksimāli 14 elektroni.
Katru orbitāli raksturo magnitūdas kvantu skaitlis ml, bet vienā orbitālē var atrasties ne vairāk kā divi elektroni ar pretējiem spin kvantu skaitļiem ms (Pauli princips).
Elektronu skaits apvalkā
Maksimālais elektronu skaits, kas var atrasties apvalkā ar galveno kvantu skaitli n, ir vienāds ar 2 n 2 {\displaystyle 2n^{2}}. 
- n = 1 (K-čaula): 2·1² = 2 elektroni;
- n = 2 (L-čaula): 2·2² = 8 elektroni;
- n = 3 (M-čaula): 2·3² = 18 elektroni.
Elektronu konfigurācija un pamatlikumi
Elektronu izvietojumu pa apvalkiem un apakščaulām apraksta elektronu konfigurācija. Konfigurāciju nosaka kvantu mehānikas principi un daži heuristiski noteikumi, ko izmanto ķīmijā un fizikā:
- Aufbau princips: elektroni aizpilda orbitāles pēc enerģijas — zemākas enerģijas orbitāles tiek aizpildītas pirmās. Tā izrietošā secība (aptuveni): 1s < 2s < 2p < 3s < 3p < 4s < 3d < 4p utt.;
- Pauli princips: vienā orbitālē var atrasties ne vairāk kā divi elektroni ar pretējiem spin kvantiem;
- Hundas likums: apakšlīmeņa orbitāles vienā enerģijas līmenī vispirms tiek viennozīmīgi apdzīvotas ar vienādiem spin, pirms notiek spina pārošanās.
Piemēri
Daži tipiski konfigurāciju piemēri:
- Ogļskābe (C), Z = 6: 1s2 2s2 2p2 — divi elektroni 1. apvalkā, četri ārējā (valences) apvalkā;
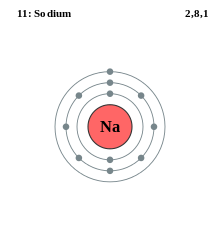
- Nātrijs (Na), Z = 11: 1s2 2s2 2p6 3s1 — viens valentais elektrons apvalkā n = 3;
- Argons (Ar), Z = 18 (pilns apvalku komplekts): 1s2 2s2 2p6 3s2 3p6 — stabila pilna apvalku konfigurācija.
Saikne ar Bohru modeli un kvantu mehāniku
Termins "čaula" cēlies no Bora modeļa, kurā elektroni it kā riņķoja ap kodolu noteiktās trajektorijās («čaulās»). Mūsdienu kvantu mehānika labāk apraksta elektronu kā viļņu-funkcijas un orbitāles — reģionus ar lielāku varbūtību atrast elektronu — nevis stingri noteiktas klasiska tipa orbītas. Tomēr čaulu ideja joprojām ir ērts un praktisks veids klasificēt un saprast elektronu izvietojumu atomā.
Ķīmiskā nozīme
Elektronu apvalki un īpaši ārējais (valences) apvalks nosaka elementu ķīmiskās īpašības — ķīmiskos saites veidus, oksidācijas stāvokļus un reakciju spējas. Apvalku aizpildījums ietekmē arī jonizācijas enerģiju, elektronegativitāti, aizsargājošu (screening) un efektīvo nukleāro lādējumu, kas ietekmē elektronu saistību ar kodolu.
Jāņem vērā
- Praktiskos aprēķinos bieži lieto īsinājumus (piem., "nātrijs: [Ne] 3s1" — ar neona konfigurāciju kā kodolu).
- Dažiem elementiem (īpaši pārejas metāliem un aktinoīdiem) konfigurācijas var atšķirties no vienkāršās Aufbau secības, jo enerģijas starp apakšlīmeņiem ir ļoti tuvas.
Apkopojot — elektronu apvalks ir pamatjēdziens, kas savieno atomu kvantu mehānisko uzbūvi ar ķīmisko uzvedību: tas ietver galvenā kvantu skaitļa noteikto enerģijas līmeni, apakšlīmeņus (s, p, d, f), orbitāles un to aizpildīšanas noteikumus, kā arī praktiskas sekas atomu īpašībām un ķīmiskajām reakcijām.