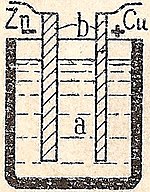
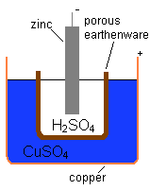
Ķīmiskā šūna pārvērš ķīmisko enerģiju elektriskā enerģijā. Lielākā daļa bateriju ir tieši tādas ķīmiskās šūnas — tajās notiek ķīmiska reakcija, kas rada elektriskās strāvas plūsmu. Akumulators ir ierīce, kas satur vienu vai vairākas šādas šūnas un nodrošina elektrību dažādiem patērētājiem.
Komponentes un darbības princips
Katra akumulatora pamatā ir trīs galvenās sastāvdaļas: anods (negatīvais elektrods), katods (pozitīvais elektrods) un elektrolīts (viela, kas vada jonu plūsmu). Izlādes laikā notiek oksidēšanās pie anoda un reducēšanās pie katoda — šo ķīmisko pārmaiņu rezultātā elektroni plūst caur ārējo ķēdi no anoda uz katodu, radot elektrisko strāvu. Uzlādes laikā, ja tā ir iespējama, ārējā strāva spiež ķīmiskās reakcijas pretējā virzienā un atjauno sākotnējos materiālus.
Akumulatoru veidi
Vispārīgi akumulatorus iedala divās grupās:
- Neuzlādējami (primārie) — vienreizlietojami: nodrošina elektrību, līdz iekšējo ķīmisko vielu potenciāls ir izlietots, un pēc tam tos vairs nevar atjaunot. Tos bieži sauc par "izmanto un izmet". Piemēri: dažas litija primāršūnas un tradicionālās sārmu baterijas.
- Uzlādējami (sekundārie) — tos var uzlādēt, caur tiem caurlaižot elektrisko strāvu pretējā virzienā, tādējādi atjaunojot sākotnējo ķīmisko stāvokli. Tipiski piemēri: svina-skābes akumulatori (automašīnās), NiCd, NiMH un mūsdienu litija jonu (Li-ion) akumulatori. Uzlādējamās baterijas pirmo praktisko veidu 1859. gadā izgudroja franču inženieris Gaston Planté.
Biežāk izmantotās ķīmijas un to īpašības
- Svina-skābes (lead-acid) — lētas, spēj dot lielu sākotnējo strāvu (piem., auto startēšanai), bet smagas un ar ierobežotu ciklu skaitu.
- NiCd (nikls-kadmijs) — izturīgas pret lielām slodzēm un temperatūras svārstībām, bet satur toksisku kadmiju un ir pakļautas atmiņas efektam.
- NiMH (nikls-metālu hidrīds) — augstāka ietilpība nekā NiCd un mazāks videi kaitīgs efekts, bet joprojām ar salīdzinoši paaugstinātu pašizlādi.
- Li-ion (litija jonu) — augsta enerģijas blīvuma, zems svars, ilgs kalpošanas laiks un plašs pielietojums (telefoni, portatīvās ierīces, elektromobiļi). Nepieciešama aizsardzība pret pārlādēšanu un pārkaršanu.
- Alkaliskās (sārmu) — parasti neuzlādējamas (ir arī uzlādējamas versijas), piemērotas ikdienas ierīcēm: tālvadības pultis, pulksteņi u.c.
Galvenie parametri un ko tie nozīmē
- Spriegums (V) — atšķirīgām ķīmijām ir raksturīgs nominālais spriegums (piem., alkaliskajām šūnām ~1,5 V, NiMH/NiCd ~1,2 V, Li-ion ~3,6–3,7 V, svina-skābes ~2 V uz šūnu).
- Jauda / ietilpība (mAh vai Ah) — norāda, cik ilgi akumulators var piegādāt noteiktu strāvu; lielāka vērtība nozīmē ilgāku darbību vienā uzlādes/izlādes ciklā.
- Iekšējā pretestība — ietekmē sprieguma kritumu pie lielām slodzēm; zema iekšējā pretestība nozīmē labāku spēju piegādāt lielas strāvas.
- Pašizlāde — līmenis, cik ātri akumulators zaudē uzlādētību stāvoklī bez pieslēgtas slodzes.
- Ciklu skaits — cik reizes akumulators var tikt pilnībā uzlādēts un izlādēts, pirms tā ietilpība kļūst būtiski mazāka.
- Dziļā izlāde (DoD) — cik liela daļa enerģijas tiek izņemta no akumulatora; daudziem akumulatoriem bieža pilna izlāde samazina kalpošanas laiku.
Drošība un pareiza lietošana
Akumulatori var būt bīstami, ja netiek izmantoti pareizi. Daži pamatprincipi:
- Izmantojiet tikai atbilstošu lādētāju, kas paredzēts konkrētajai ķīmijai un baterijas tipam; pareizs uzlādes režīms pagarina kalpošanas laiku un novērš bojājumus.
- Nekad neīstenojiet īssavienojumu starp akumulatora spailēm — tas var izraisīt dzirksteles, siltumu un bojājumus.
- Neatstājiet litija jonu akumulatorus pārkarstam vai tiešā saulē; pārmērīga temperatūra var izraisīt termālu nestabilitāti (thermal runaway).
- Nepārdzīvojiet akumulatoru mehāniski — bojājumi var izraisīt noplūdes vai ugunsrisku.
Atkritumu apsaimniekošana un pārstrāde
Akumulatori satur materiālus, kas var būt videi kaitīgi (svins, kadmijs, liels litija daudzums u.c.). Tāpēc tos nedrīkst izmest sadzīves atkritumos. Nododiet izlietotās baterijas speciālās vākšanas vietās vai pārstrādes punktos. Pārstrāde ļauj iegūt vērtīgas izejvielas un samazina vides piesārņojumu.
Pielietojumi
Akumulatori tiek izmantoti ļoti plašā jomu spektrā: ikdienas sīkrīki (telefoni, portatīvie datori), rotaļlietas, fotoaparāti, viedierīces, automašīnas (startēšana, hibrīdiekārtas, elektromobiļi), rūpniecības enerģijas uzkrāšana un pat zemūdenēs un citos lielos transportlīdzekļos. Izvēle starp dažādām akumulatoru tehnoloģijām balstās uz vajadzīgo enerģijas blīvumu, izmaksām, drošību un ekspluatācijas prasībām.
Apkopojot: akumulators ir ķīmiskā šūna vai šūnu grupa, kas pārveido ķīmisko enerģiju elektrībā. Sapratne par to darbības principiem, ķīmijām, parametriem un drošības prasībām palīdz izvēlēties pareizo bateriju konkrētam pielietojumam un pareizi to lietot, uzturēt un utilizēt.