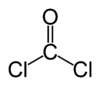
Fosgēns ir ķīmisks savienojums ar formulu COCl2 . Šai gāzei nav krāsas. Šo gāzi izmantoja kā ieroci Pirmā pasaules kara laikā. Tā ir atbildīga par lielāko daļu nāves gadījumu, kas saistīti ar indīgo gāzi kara laikā. Mūsdienās fosgēnu izmanto kā instrumentu. To izmanto organiskajā sintēzē. Ja gaisā ir neliels daudzums, smarža ir līdzīga svaigi nopļauta siena vai zāles smaržai. Daži karavīri Pirmā pasaules kara laikā ir apgalvojuši, ka tā smarža nedaudz atgādināja maija ziedu smaržu. Kad daži hlora savienojumi deg vai sadalās, izdalās neliels daudzums fosgēna.
Vēsture
Fosgēns tika identificēts 19. gadsimtā kā ķīmisks savienojums, bet plašu bīstamību un potenciālu lietošanai kā kaujas gāze tas ieguva Pirmā pasaules kara laikā. Fosgēns tika izmantots kā knaibljošs (choking) aģents — tieša iedarbība uz elpošanas sistēmu nereti izraisīja nomākumu plaušās un smagu plaušu tūsku, kas bieži bija nāvējoša. Pēc kara šī gāze turpināja būt nozīmīga ķīmiskās rūpniecības izejviela, taču tās izmantošana un tirdzniecība ir stingri reglamentēta drošības apsvērumu dēļ.
Fizikālās un ķīmiskās īpašības
- Vienādojums: COCl2.
- Izskats: bezkrāsaina gāze vai aromātiskais šķidrums zem spiediena vai zemā temperatūrā.
- Smarža: pie maziem koncentrāciju slāņiem var atgādināt svaigi nopļautu sienu vai zāli; tomēr olfaktors var apmānīt — pie lielākiem daudzumiem smaka var nebūt jūtama un var rasties olfaktora nogurums.
- Bīstamība: ļoti toksisks; iedarbojas galvenokārt uz elpošanas ceļiem un plaušām.
- Ķīmiskā reaktivitāte: reaģē ar ūdeni, hidrolizējas uz oglekļa dioksīdu (CO2) un sālsskābi (HCl): COCl2 + H2O → CO2 + 2 HCl.
- Vide: mitrā vidē ātri sadalās; sausā atmosfērā var saglabāties ilgāk.
Ražošana un rūpnieciskā izmantošana
Rūpnieciski fosgēns parasti tiek ražots, oksidējot oglekļa monoksīdu (CO) ar hlora gāzi (Cl2) uz katalizatora vai ar citām ķīmiskām metodēm. Tas ir svarīgs starpprodukts organiskajā sintēzē:
- ražošanai isikānātu un karbamītu atvasinājumiem;
- ražošanai karbamoilhlorīdu un skābes hlorīdu sintēzei;
- speciālajā organiskajā sintēzē kā karbonilēšanas līdzeklis.
Rūpnieciskās izmantošanas dēļ fosgēna ražošana, uzglabāšana un transportēšana tiek veikta ar īpašiem drošības pasākumiem.
Bīstamība un veselības ietekme
Fosgēns ir ļoti toksisks un var radīt nopietnas veselības problēmas pat īsas ekspozīcijas gadījumā. Tipiskie simptomi:
- acu un acu gļotādu, deguna un rīkles kairinājums, sāpes acīs;
- klepus, elpas trūkums, švīkstoša elpošana;
- novēlota iedarbība — simptomi var pasliktināties pēc stundām līdz pat dienai, izraisot plaušu tūsku (pulmonālu edēmu);
- augstas koncentrācijas var izraisīt ātru elpošanas mazspēju un nāvi.
Nav specifiska universāla "pretinde" fosgēnam; medicīniskā palīdzība parasti ir atbalstoša — skābekļa terapija, elpošanas atbalsts un simptomi ārstēšana.
Avāriju novēršana, atklāšana un pirmā palīdzība
- Novēršana: rūpnieciskajās iekārtās jāizmanto slēgta sistēma, attiecīgi pretplūsmas filtri, gāzu detektori un darbinieku apmācība.
- Detektēšana: speciāli gāzu detektori un monitori ir obligāti, jo cilvēka oža nedod drošu aizsardzību (smaka var nebūt pamanāma vai var apmānīt).
- Pirmā palīdzība: ja cilvēks bija pakļauts iedarbībai — nekavējoties nogādāt svaigā gaisā, noņemt piesārņotu apģērbu, skartās vietas skalot ar lielu daudzumu ūdens (acis un āda), nodrošināt medicīnisku novērošanu vismaz 24–48 stundas, jo elpošanas simptomi var attīstīties aizkavēti. Snaudēšanas, vemšanas vai bezsamaņas gadījumos nekavējoties izsaukt neatliekamo palīdzību.
Vides jautājumi un regulācija
Fosgēns vājā ūdens vide ātri hidrolizējas, tāpēc tas parasti ilgi neuzkrājas dabā, tomēr izmeši gaisā var būt bīstami teritorijām ap rūpnīcām. Izmešu, ražošanas un transportēšanas drošības prasības ir stingras; fosgēna izmantošana ir regulēta gan nacionālā, gan starptautiskā līmenī. Tā kā fosgēns vēsturiski tika izmantots kā kaujas gāze, tā izmantošana militāros nolūkos ir aizliegta un jebkura vardarbīga pielietojuma potenciāla novēršana ir starptautisks jautājums.
Svarīgi atcerēties
- Fosgēns ir bezkrāsaina, ļoti toksiska gāze ar raksturīgu pie maziem koncentrācijas līmeņiem atgādinošu smaržu, taču izjūtas var maldināt.
- Pat ja sākotnējie simptomi šķiet viegli, iespējama novēlota un smaga plaušu bojājuma attīstība — nepieciešama medicīniska novērošana.
- Rūpnieciskā darbība un transportēšana notiek ar stingriem drošības pasākumiem, un jebkura avārija prasa tūlītēju speciālistu iesaisti.