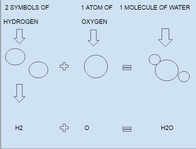
Ķīmiskā formula ir veids, kā ķīmiķi apraksta molekulu. Formulā ir norādīts, kādi atomi un cik daudz katra veida atomu ir molekulā. Dažreiz formulā ir norādīts, kā atomi ir saistīti, un dažreiz formulā ir norādīts, kā atomi ir izvietoti telpā.
Burts norāda, kāds ķīmiskais elements ir katrs atoms. Apakšindekss norāda katra atoma veida skaitu. Piemēram, ūdeņraža peroksīda formula ir H2 O2 . Metānam ir viens oglekļa (C) atoms un četri ūdeņraža atomi; ķīmiskā formula ir CH4 . Cukura molekulā glikozei ir seši oglekļa atomi, divpadsmit ūdeņraža atomi un seši skābekļa atomi, tāpēc tās ķīmiskā formula ir C 6H 12O 6.
Ķīmiskās formulas tiek izmantotas ķīmiskajos vienādojumos, lai aprakstītu ķīmiskās reakcijas.
Šo ķīmisko formulu rakstīšanas sistēmu izstrādāja 19. gadsimta zviedru ķīmiķis Jonss Jēkabs Bērzeliuss.
Ko attēlo ķīmiskā formula?
Ķīmiskā formula sniedz vienkāršu raksturojumu par savienojuma ķīmisko sastāvu. No tās var uzzināt:
- Elemntu sastāvu: kuri elementi un cik katra veida atomi atrodas molekulā (piem., C6H12O6).
- Stöhiometriju: attiecības starp atomiem reakcionējošās vielās un produktos, kas svarīgi ķīmisko vienādojumu līdzsvarošana.
- Jonu lādiņus un grupas: jonu savienojumos parasti tiek norādīts lādiņš, piemēram Na+ vai SO42−.
- Saistību grupa vai struktūra: daļēji atklāt ar strukturālām formulām vai ariekavām, piemēram (NH4)2SO4.
Formulu veidi
- Molekulārā formula — rāda faktisko atomu skaitu molekulā (piem., H2O, CO2, C6H12O6).
- Empīriskā (relatīvā) formula — vienkāršākais attiecību attēlojums starp elementiem (piem., glikozes empīriskā formula ir CH2O).
- Strukturālā formula — parāda atomu savienojumu secību un saišu tipa, bieži izmantojot līnijas, bultas vai kondensētu syntaksi (piem., CH3CH2OH vietā C2H5OH).
- Condensed (kondensētā) formula — kompaktāks strukturālās informācijas veids (piem., CH3CHClCH3).
- Jonu un formula vienības — jonu savienojumiem norāda katru jonu un to attiecības (piem., NaCl, CaCO3).
- Izotopu notācija — norāda konkrētā izotopa masas skaitli, piemēram 14C vai 2H (D).
Simboli un rakstības noteikumi
- Elementu simboli — katram elementam ir viena vai divu burtu simbols (C, O, Na, Cl).
- Apakšindekss (subscript) — norāda atomu skaitu konkrētajā molekulā, piemēram H2, O2.
- Priekšā esošie koeficienti — norāda molekulu skaitu vienā reakcijā: 2 H2 + O2 → 2 H2O.
- Iekavas — lieto, ja vienā grupā ir vairāki atomu komplekti, piemēram (NH4)2SO4.
- Superskripts — jonos norāda lādiņus, piemēram Ca2+, Cl− vai SO42−.
- Stāvokļa simboli — reakciju vienādojumos bieži pievieno (s), (l), (g), (aq) — cietā, šķidrā, gāzveida, šķīdumā.
Praktiski piemēri
- Ūdens: H2O — viens skābekļa atoms un divi ūdeņraža atomi.
- Ūdeņraža peroksīds: H2O2 — uzrāda divas OH vienības, molekulā divi O un divi H.
- Metāns: CH4 — viens C un četri H.
- Nātrija hlorīds: NaCl — joniska formula, viena Na+ un viena Cl−.
- Ammonija sulfāts: (NH4)2SO4 — piemērs, kur jālieto iekavas un apakšindekss.
- Reakciju piemērs: 2 H2 + O2 → 2 H2O — rāda stoihiometriju.
Strukturāla informācija un stereoķīmija
Dažas formulas tikai norāda sastāvu, bet nevar atšķirt izomērus (vielas ar vienādu molekulāro formulu, bet atšķirīgu struktūru). Lai to parādītu, izmanto:
- Strukturālās formulas, kas rāda saites starp atomiem.
- Lewis struktūras, kas parāda valentielektronu pārus.
- Stereokīmiskās notācijas (wedges/dashes, E/Z, R/S), lai norādītu telpisko atomu izvietojumu un konfigurāciju.
Kā formulas izmanto ķīmijā
- Stöhiometrijas aprēķini: no formulām var aprēķināt molu attiecības un vielas daudzumus reakcijās.
- Molarā masa: summējot atomu relatīvās masas pēc formulām, nosaka viena mols vielas masu (g/mol).
- Reakciju raksturošana: formulas tiek lietotas ķīmiskajos vienādojumos, lai parādītu reaģentu un produktu sastāvu.
Biežas kļūdas un padomi
- Atcerieties, ka apakšindeksi attiecas tikai uz tieši pirms tiem esošajiem elementiem vai grupām: H2O nozīmē divus H uz katru O.
- Neaizmirstiet par koeficientiem reakcijās — tie norāda molekulu skaitu, nevis atomu skaitu molekulā.
- Lai noteiktu faktisko struktūru (īpaši organiskajos savienojumos), bieži nepieciešama strukturālā vai stereokīmiskā formula, ne tikai molekulārā formula.
Ķīmiskās formulas ir vienkāršs, bet jaudīgs instruments gan skolās, gan pētījumos un rūpniecībā — tās ļauj ātri saprast vielas sastāvu, aprēķināt reaksiju sastāvu un sazināties precīzi par ķīmiskajiem procesiem.