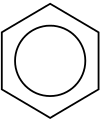
Aromātiskais ogļūdeņradis jeb arēns ir ogļūdeņraža gredzena savienojums. Tam raksturīgas mainīgas dubultās un vienkāršās saites starp oglekļa atomiem, kas veido gredzenus, un parasti pastāv π-elektronu delokalizācija — elektronus var attēlot kā sadalītus pāriem pāri pār visu gredzenu, nevis atsevišķu saišu vietās. Daudziem aromātiskajiem savienojumiem piemīt raksturīgs saldeni asais aromāts, no tā arī nosaukums "aromātisks". Aromātisko savienojumu gredzenu no sešiem oglekļa atomiem sauc par benzola gredzenu pēc visvienkāršākā iespējamā ogļūdeņraža — benzola — vārda. Aromātiskie ogļūdeņraži var būt monocikliski (MAH) vai policikliski (PAH).
Elektronu delokalizācija un stabilitāte
Aromātiskuma pamatā ir delokalizētu π-elektronu sistēma, kas piešķir īpašu stabilitāti. Saskaņā ar Hikla noteikumu (Hückel) par aromātismu, cik vienkārši izsakoties, plakanai cikliskai sistēmai ir aromātiskas īpašības, ja tajā ir (4n + 2) delokalizētu π-elektronu (n ir vesels skaitlis). Piemēram, benzolam n = 1, tāpēc tam ir 6 π-elektroni un tas ir aromātisks. Aromātiskums izpaužas arī kā vienādas saišu garuma starpība un lielāka reaktivitātes un stabilitātes atšķirība pret parastajām alkēnu dubultsaitēm — aromātiskie gredzeni ir mazāk viegli pieejami pievienošanās reakcijām, bet tie aktīvi piedalās elektrofilā aromātiskā substitūcijā (piem., nitrācija, halogenēšana, sulfonēšana, Friedel–Crafts reakcijas).
Policikliskie aromātiskie ogļūdeņraži (PAH)
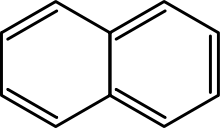
PAH ir vairāku saplūdušu aromātisko gredzenu savienojumi, piemēram, naftalīns, antracēns, fenantrēns. Tie rodas dabiski un antropogēniski — no nepilnīgas organisko materiālu sadedzināšanas (piem., kokogles, cigarešu dūmi, automašīnu izplūdes gāzes, rūpnieciskie procesi). PAH īpašības:
- parasti lipofīli (slikti šķīst ūdenī),
- persitentāri vidē — var uzkrāties augsnē un nogulumos,
- daudzi ir mutagēni un karcinogēni (piem., benzo[a]pirēns),
- to bioloģiskā aktivitāte un toksicitāte atkarīga no struktūras un substituentiem.
Heteroarēni
Daži savienojumi, kas nav vienkārši benzola atvasinājumi, tomēr ir aromātiski — tos sauc par heteroarēniem. Šajos savienojumos vismaz viens oglekļa atoms ir aizstāts ar citu elementu, visbiežāk skābekļa, slāpekļa vai sēra atomu. Tipiski piemēri ir:
- pirimidīns, piridīns — slāpekļa saturoši aromāti;
- furāns — skābekļa saturošs piecu locekļu aromātisks gredzens;
- tiolfēns (tiophene) — sēra saturošs piecu locekļu aromāts;
- pirrols — slāpekli saturošs piecu locekļu aromāts, kur slānekļa iekšējais H iesaistās π-sistēmā.
Heteroarēniem aromātiskums arī atbilst Hikla noteikumam, taču elektronu skaitīšana un reakciju reaktivitāte var atšķirties atkarībā no heteroatomu dabas (elektronu donora vai akceptora īpašības).
Reakcijas un ķīmiskā uzvedība
Benzola tipa aromāti parasti piedalās elektrofilā aromātiskā substitūcijā, kur elektrofilais reagents aizstāj šķīduma atomu vai grupu gredzenā, nevis pievienojas dubultsaišu veidā. Substituentu elektronu donora vai akceptora raksturs ietekmē to, kurā pozīcijā (ortho / meta / para) jauns grupējums pārsvarā tiks ievietots. Policikliski aromātiskie ogļūdeņraži var piedalīties arī oksidācijas, cīnīšanās un dimerizācijas reakcijās augstākās temperatūrās vai radikālu apstākļos.
Fizikālās īpašības un pielietojums
Aromātiskie savienojumi bieži ir šķidrumi vai cietas vielas ar salīdzinoši augstu blīvumu un specifisku smaržu. Benzols un tā atvasinājumi tiek plaši izmantoti kā organiski šķīdinātāji, ķīmiskās ražošanas izejvielas (piem., polimēru, krāsvielu, medikamentu sintezē), kā arī degvielas komponentes. PAH tiek pētīti gan kā potenciāli vērtīgi organiskie materiāli (piem., organiskās elektronikas, optoelektronikas komponentes), gan kā vides un veselības risks.
Vides un veselības aspekti
Daudzi PAH ir toksiski, mutagēni un dažiem ir pierādīta kancerogēna iedarbība uz cilvēkiem un dzīvniekiem. Tie var iekļūt organismā caur ieelpošanu (dūmi, benzīna izplūdes), norīšanu (piesārņots pārtikas produkts) vai caur ādu. Vides piesārņojums ar PAH ir svarīgs jautājums — tiek veikta monitorēšana, samazināšanas un attīrīšanas prakse, lai mazinātu ekspozīciju. Arī daži vienkāršie aromātiskie šķīdinātāji (piem., benzols) ir toksiski un karcinogēni, tāpēc to lietošana ir regulēta.
Kopsavilkums
Aromātiskie ogļūdeņraži (arēni) ir īpaša organiska ķīmijas klase, kurai raksturīga delokalizēta π-elektronu sistēma un lielāka stabilitāte. Tie ietver vienkāršus benzola atvasinājumus, plaši policiklus savienojumus (PAH) un heteroarēnus, kuros gredzenu veido arī citi elementi. Aromātiskie savienojumi ir chemiski nozīmīgi un plaši pielietoti, taču tie var radīt arī būtiskus veselības un vides riskus, īpaši attiecībā uz noteiktiem PAH un benzola veidiem.