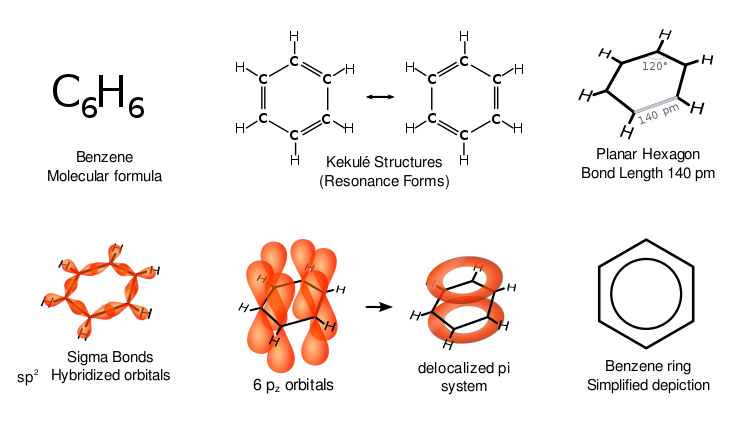Benzols, pazīstams arī kā benzols, ir organisks ķīmisks savienojums ar formulu 6CH6. Tas ir bezkrāsains un viegli uzliesmojošs šķidrums ar saldu smaržu. Benzola molekulas ir gredzens no sešiem oglekļa atomiem, kas katrs ir saistīts ar vienu ūdeņraža atomu. Tas ir aromātisks savienojums, kas nozīmē, ka gredzenam ir mainīgas dubultās saites.
Benzols ir kancerogēns, kas nozīmē, ka tas var izraisīt vēzi. Tam ir daudz reālu pielietojumu. To izmanto kā piedevu benzīnam, plastmasai, sintētiskajam kaučukam, krāsvielām, un tas ir rūpniecisks šķīdinātājs, kas nozīmē, ka tas var izšķīdināt daudzas citas ķīmiskas molekulas. Benzols ir arī dabiska jēlnaftas sastāvdaļa, tāpēc tas ir benzīna sastāvā. Daudzu zāļu sastāvā ir no benzola izgatavotas daļas.
Fizikālās un ķīmiskās īpašības
- Stāvoklis: bezkrāsains, eļļains šķidrums istabas temperatūrā.
- Smarža: salda, raksturīga aromātiska smarža (jutība smakai atšķiras starp cilvēkiem).
- Uzliesmojamība: viegli uzliesmojošs — tvaiki var veidot sprādzienbīstamas maisījumus ar gaisu.
- Šķīdība: praktiski nešķīst ūdenī, labi šķīst organiskos šķīdinātājos.
- Ķīmiskā īpašība: aromātiskais oglekļa gredzens dod benzolam raksturīgo stabilitāti, tomēr tas reaģē ar elektrofīliem papildinājumiem un oksidēšanos.
Kur benzols rodas un kā to ražo
- Dabā benzols sastopams jēlnaftā un tiek izdalīts no degšanas procesiem (piem., automašīnu izplūdes gāzes, ugunsgrēki).
- Rūpniecībā benzolu iegūst no naftas frakcionēšanas un no aromātu pārstrādes procesiem. To var iegūt arī sintētiski no acetilēna vai citiem izejmateriāliem.
Lietojumi
Benzols ir izejmateriāls daudzos rūpnieciskos procesos un produktos:
- Kā izejviela organisko savienojumu sintezē: krāsvielas, smaržvielas, detergenti, farmaceitiskie produkti.
- Kā rūpnieciskais šķīdinātājs organiskajām vielām (tomēr drošāki aizstājēji tiek izmantoti, jo benzols ir toksisks).
- Kā sastāvdaļa degvielā — benzīna frakcijās; daļēji tiek pievienots kā antidetonants vai aromāts, bet izmantošana tiek ierobežota veselības dēļ.
- Rūpnieciskās ķīmijas ražošanā: sintētiskā kaučuka, plastmasas, krāsvielu un dažu zāļu starpproduktu ražošana.
Veselības riski un toksikoloģija
Akūta iedarbība: īslaicīga lielu benzola tvaiku ieelpošana var izraisīt galvassāpes, reiboni, nelabumu, reibumu, miegainību un samaņas zudumu. Augstas koncentrācijas var bojāt centrālo nervu sistēmu un izraisa elpošanas traucējumus vai sirds darbības traucējumus.
Kroniska iedarbība: ilgstoša ekspozīcija (galvenokārt darbā) var bojāt kaulu smadzenes, izraisot anēmiju, leikopēniju un citus asinsainas traucējumus. Benzols ir saistīts ar paaugstinātu risku attīstīt akūtu mielolīzi vai akūtu mieloīdo leikēmiju (AML). Tā dēļ benzols tiek klasificēts kā kancerogēns.
Jutīgākās grupas: bērni, grūtnieces un cilvēki ar hematopoētiskās sistēmas traucējumiem var būt īpaši jutīgi pret benzola iedarbību.
Ekspozīcijas ceļi un vide
- Ieelpošana — visizplatītākais risks: benzola tvaiki ātri iekļūst asinīs un izplatās organismā.
- Ādas kontakts — var notikt uzsūkšanās caur ādu, īpaši ilgstošs kontakts vai šķidrumu izlijumi bez aizsardzības.
- Norīšana — reti, bet bīstami; var notikt darba vietās vai avārijas situācijās.
- Vides piesārņojums — benzols var iekļūt gruntsūdeņos un augsnē, ilgstoši ietekmējot ūdens kvalitāti un ekosistēmas.
Noteikumi, robežvērtības un drošības vadlīnijas
Daudzas valstis ir ieviesušas darba vides un vides robežvērtības benzola koncentrācijai gaisā un ūdenī. Darba vietās tiek prasīts samazināt ekspozīciju ar tehniskajiem pasākumiem, ventilāciju un personīgo aizsardzību. Pārbaudiet vietējos normatīvus un ieteikumus, jo robežvērtības un vadlīnijas var atšķirties.
Monitoring un analīze
Benzolu atklāj ar gāzu monitoriem, personīgajiem uzraudzības ierīcēm, kolorimetriskajām testu caurulītēm, un laboratorijas analīzēm (piem., gāzu hromatogrāfija ar masas spektrometriju). Regulāra monitoringa veikšana darba vietās un piesārņotās vides pārbaude palīdz novērst pārmērīgu iedarbību.
First aid un drošības pasākumi
- Ja ieliet vai uzkrita uz ādas: noņemt piesārņotu apģērbu un ātri nomazgāt ādu ar ūdeni un ziepēm; meklēt medicīnisku palīdzību, ja rodas kairinājums vai simptomi.
- Ja nokļuvis acīs: skalot acis ar tīru tekošu ūdeni vismaz 15 minūtes un nekavējoties meklēt medicīnisku palīdzību.
- Ja ieelpots: nogādāt personu svaigā gaisā, nodrošināt atpūtu; ja elpošana apstājas — veikt elpināšanu; sazināties ar neatliekamās medicīniskās palīdzības dienestu.
- Saindēšanās gadījumā ar norīšanu: nekavējoties zvanīt mediķiem; neizraisīt vemšanu, ja nav norādījuma no speciālista.
- Ugunsgrēka gadījumā: benzola liesmas slāpē ar putu, sausajiem ķīmiskajiem vai CO2 slāpētājiem; izvairīties no ūdens strūklas, kas var izplatīt izlieto vielu.
Samazināšana un aizstājēji
Rūpniecībā un laboratorijās tiek meklēti drošāki šķīdinātāji un izejvielas, lai aizstātu benzolu. Izmantošanas samazināšana, aizsargaprīkojums (respiratori, ķimikāliju izturīgs apģērbs) un tehniskie pasākumi (slēgtas sistēmas, ventilācija) būtiski samazina risku.
Secinājums
Benzols ir daudzpusīgs organiskais savienojums ar svarīgiem rūpnieciskajiem pielietojumiem, taču tas ir bīstams cilvēku veselībai un videi. Pareiza darba aizsardzība, rūpīga monitoringa prakse un alternatīvu izmantošana ir svarīgi, lai samazinātu ekspozīcijas riskus. Ja ir aizdomas par benzola iedarbību vai piesārņojumu, sazinieties ar veselības aprūpes speciālistu vai attiecīgajām vides/ darba aizsardzības institūcijām.

_1964,_MiNr_440.jpg)