Atomteorija ķīmijā un fizikā izskaidro, kā laika gaitā mainījusies mūsu izpratne par atomu. Kādreiz atomus uzskatīja par mazākajiem vielas gabaliņiem. Tomēr tagad ir zināms, ka atomi sastāv no protoniem, neitroniem un elektroniem. Šīs subatomārās daļiņas savukārt sastāv no kvarkiem un mijiedarbojas caur spēcīgajām un vājajām kodolspējām. Pirmo ideju par atomu radīja grieķu filozofs Demokrīts, bet daudzas mūsdienu teorijas pamatidejas formulēja britu ķīmiķis un fiziķis Džons Daltons.
Šī teorija attiecas uz cietām vielām, šķidrumiem un gāzēm, bet tā nav analoga plazmai vai neitronu zvaigznēm. Plazma ir jonizēta gāze, kur atomi ir sadalīti uz joniem un brīviem elektroniem, savukārt neitronu zvaigznes satur ārkārtīgi blīvu kodolmateriālu, kur parastā atoma struktūra vairs nepiemērojas.
Vēsturiskā attīstība
Atomteorijas attīstība iet cauri vairākiem svarīgiem posmiem:
- Antīkā doma: Demokrīta un citu domu skolas idejas par nedalāmu vielas daļu;
- Daltona modelis: ķīmiskie likumi un ideja par elementu atomiem ar noteiktu masu;
- J. J. Tomsona modelis: atklāja elektronu un ierosināja “raisītes” (plum pudding) modeli;
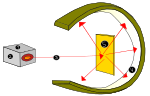
- Rutherforda izkliedes eksperiments: parādīja, ka atoma masa koncentrēta mazā, pozitīvā kodolā;
- Bora modelis: kvantizētas elektronu orbītas, kas izskaidroja spektrus;
- Kvantmehānika: Šrēdingera viļņu funkcija, Haizensberga nenoteiktības princips un mūsdienu orbitalu koncepcija.
Atoma uzbūve un galvenie jēdzieni
Atoma galvenie komponenti ir kodols un elektronmākonis. Kodolā atrodas protoni (pozitīvi lādēti) un neitroni (neitrāli). Elektroni (negatīvi lādēti) kustas ap kodolu, veidojot blīvu elektronu mākoni, kurā izpaužas varbūtības sadalījums par elektronu esamību konkrētā vietā. No svarīgākajiem jēdzieniem:
- Atoma numurs (Z): protonu skaits kodolā — nosaka elementa ķīmiskās īpašības;
- Masa skaitlis (A): protonu un neitronu kopskaits — nosaka izotopu masu;
- Orbitalas un enerģijas līmeņi: elektroni aizņem orbitālas ar noteiktām enerģijām, kas nosaka ķīmiskās saites;
- Pauli princips: katru kvantu stāvokli var aizņemt ne vairāk kā viens elektrons ar konkrētu spin vērtību.
Subatomārās daļiņas, kvarki un kodoldalības
Protoni un neitroni nav fundamentālas daļiņas — tie sastāv no kvarkiem, kurus savieno gluoni, kas pārraida spēcīgo mijiedarbību. Ir trīs “krāsas” kvarku mijiedarbībai un dažādi kvarku veidi (up, down, strange u.c.), kas skaidro hadronu īpašības. Kodolā darbojas arī vājā mijiedarbība (radojot radioaktīvos procesus) un elektromagnētiskā mijiedarbība starp lādiņiem.
Eksperimentālie pamati
Atomu un to komponentu eksperimentālais izpētes instruments ir plašs: no spektrālās analīzes, kas atklāja kvantizētus enerģijas līmeņus, līdz elektronu izkliedes eksperimentiem, rentgena kristalogrāfijai, elektronmikroskopijai un augsta enerģijas daļiņu paātrinātājiem, kas ļāva atklāt kvarkus un gluonus. Radioaktivitāte un kodolsintēze arī sniedz būtisku informāciju par kodola struktūru un spēkiem tajā.
Atomu loma ķīmijā un fizikā
Atomu īpašības un to savstarpējā mijiedarbība veido ķīmiskās saites un materiālu īpašības. Elektronu konfigurācija nosaka, kā atoms reaģēs, veidos saites un kuram vietā periodiskajā tabulā tas atrodas. Fizikā atomi ir svarīgi gan kvantu sistēmu izpētē, gan materiālu zinātnē, gan kodolfizikā un astrofizikā.
Limiti un speciālie stāvokļi
Lai gan atomu modelis skaidro lielu daļu par parastajiem materiāliem, pastāv situācijas, kur vienkāršs atoma attēlojums vairs neder: ļoti augstas temperatūras un plazmas stāvokļi, īpaši blīvas vielas (piemēram, neitronu zvaigznēs), un ļoti augstas enerģijas sadursmes, kurās rodas jaunas daļiņas. Šajās jomās nepieciešami īpaši modeļi un teorijas.
Kāpēc atomu teorija ir svarīga
Atomu teorija ir pamats, uz kura balstās ķīmija, materiālzinātne, daļiņu fizika un daudzi tehnoloģiskie risinājumi — no pusvadītājiem un medikamentiem līdz kodolenerģijai un medicīniskajai attēlveidošanai. Sapratne par atomu struktūru ļauj prognozēt un inženierēt materiālu īpašības un ķīmiskās reakcijas.
Kopsavilkumā: atomu teorija ir dinamisks jēdziens, kas savāc un izskaidro plašu datu loku — no antīkām domām līdz mūsdienu kvantu lauka teorijām. Tā palīdz izprast vielas uzbūvi un mijiedarbību gan ikdienišķos apstākļos (cietās vielas, šķidrumi, gāzes), gan ekstrēmos apstākļos, ja vien tiek pielietoti atbilstoši modeli un teorijas.