p53 (jeb tp53) ir gēns, kas ir svarīgs daudzām dzīvības formām, tostarp cilvēkam. Tas kodē olbaltumvielu, kas kavē vēža attīstību. Tas tiek dēvēts par "genoma sargsuni".
Gēns p53 ir visbiežāk mutētais gēns (> 50 %) cilvēka vēža gadījumā. Tā proteīna produkts saistās ar DNS un regulē gēnu ekspresiju, lai novērstu genoma mutācijas.
cilvēka embrionālajās cilmes šūnās (hESC) p53 proteīna (TP53) līmenis ir zems. Tas ļauj strauji noritēt svarīgākajai šūnu dalīšanās procesam.
Ko dara p53 (TP53)?
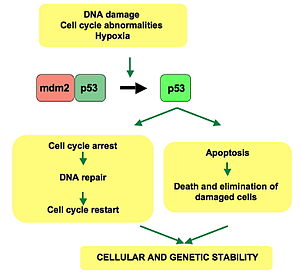
TP53 proteīns darbojas kā transkripcijas faktors — tas piesaistās noteiktām DNS secībām un ieslēdz vai izslēdz gēnus, kas kontrolē šūnas reakciju uz stresu. Galvenās p53 funkcijas:
- Šūnu cikla apturēšana — p53 aktivizē gēnus (piem., p21), kas aptur šūnu dalīšanos, dodot šūnai laiku salabot DNS bojājumus.
- Apoptoze (programmēta šūnu nāve) — ja bojājumi ir neatgriezeniski, p53 var aktivizēt apoptozi, aktivējot efektorus kā BAX, PUMA u.c., lai novērstu potenciāli vēžaizraisītas šūnas izplatīšanos.
- Šūnu senescence — p53 var izraisīt ilgtspējīgu dalīšanās spējas zudumu, kas ierobežo bojātu šūnu dalīšanos.
- DNS remonts — p53 regulē gēnus, kas piedalās DNS bojājumu atpazīšanā un labošanā.
Kā p53 tiek regulēts?
TP53 aktivitāte ir stingri kontrolēta, jo pārmērīga p53 aktivācija var traucēt normālu audu atjaunošanos. Galvenie regulatori ir:
- MDM2 — proteīns, kas saista p53, veicina tā ubiquitināciju un degradāciju. Stresa apstākļos MDM2 sadarbība tiek traucēta, ļaujot p53 uzkrāties.
- Post-translācijas modifikācijas — fosforilācija, acetilācija un citas modifikācijas maina p53 stabilitāti un transkripcijas aktivitāti.
- Isoformu un interaktoru režija — p53 eksistē vairākās formās un mijiedarbojas ar citiem proteīniem, kas ietekmē tā darbību.
Mutācijas un klīniskā nozīme
TP53 mutācijas ir ļoti biežas cilvēka audzējos. Šīs mutācijas var būt:
- Loss-of-function — samazina vai atceļ p53 aizsargfunkcijas, ļaujot bojātām šūnām pavairoties.
- Dominant-negatīvas — mutētais p53 var traucēt arī veselā allela darbību.
- Gain-of-function — dažas mutācijas piešķir jaunus, audzēju veicinošus īpašumus.
Ģenētiskas TP53 mutācijas izraisa arī reto, bet smago Li–Fraumeni sindromu, kam raksturīga agrīna un vairāku veidu ļaundabīgu audzēju attīstība.
p53 un cilmes šūnas
Embrionālajās cilmes šūnās p53 līmenis parasti ir zems, kas atvieglo aktīvu proliferāciju un pluripotenciātes uzturēšanu. Tomēr, ja hESC saskaras ar DNS bojājumiem vai citu stresu, p53 aktivācija var izraisīt diferenciāciju vai apoptozi, tādējādi novēršot bojātu šūnu nodošanu tālākajām šūnu līnijām.
Praktiskas un terapeitiskas sekas
- TP53 statusa noteikšana audzēju diagnostikā un prognozēšanā — nodrošina informāciju par slimības agresivitāti un iespējamu ārstēšanas reakciju.
- Jaunrades terapijas — pētniecība vērsta uz p53 atjaunošanu (piem., MDM2 inhibitori), mutētā p53 mērķēšanu vai p53 ceļu modulēšanu, lai pastiprinātu vēža šūnu jutību pret terapiju.
- Biomarkeri un personalizēta medicīna — TP53 mutācijas var ietekmēt izvēlēto ķīmijterapijas vai mērķterapijas efektivitāti.
Kopsavilkums
TP53 jeb p53 ir centrāla gēna/proteīna sistēma, kas darbojas kā "genoma sargs", koordinējot šūnas atbildes uz stresu, kontrolējot šūnu dalīšanos, DNS remontu un apoptozi. Tā loma padara to par kritisku elementu vēža bioloģijā, un TP53 pētniecība turpina sniegt būtiskas atziņas par diagnostiku un ārstēšanu.