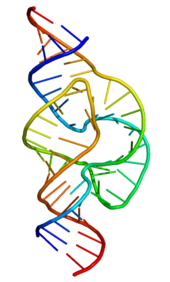
Ribozīms (ribonukleīnskābes enzīms) ir RNS molekula, kas spēj katalizēt konkrētas bioķīmiskās reakcijas tāpat kā proteīnu enzīmi. Ribozīmi izmanto RNS ķīmiskās īpašības — galvenokārt 2'-hidroksilgrupu, noteiktu bāzu konfigurāciju un metaljonu mijiedarbības —, lai paātrinātu vazariem reakciju soļus un stabilizētu pārejas stāvokļus.
Ribozīmi, ko sauc arī par katalītisko RNS, veic plašu funkciju spektru: tie darbojas ribosomā peptīdu saišu veidošanā (peptidiltransferāzes aktivitāte, ko veic rRNA), piedalās olbaltumvielu sintēzes procesā, veic RNS sazarošanu un spiešanu, kā arī dažos vīrusiem ir būtiska loma vīrusu replikācijā un pārneses RNS apstrādē un biosintēzē. Daži ribozīmi šķeļ RNS ķēdes (endonukleāzes aktivitāte), citi veic ligāciju, splicing-u vai modifikāciju reakcijas.
Struktūra un katalītiskais mehānisms
Ribozīmi parasti satur noteiktu primāro sekvenci, kas veido specifiskas otraļšķirnes un trešā līmeņa saritinājumus — cilpas, tinumus, pseidoķēdes un spilventiņu formas. Šie elementi veido katalītisku kodolu, kurā tiek koordinēti substrāti un bieži iesaistīti metālu joni (piem., Mg2+). Katalīzei var būt nozīme:
- direktai bāzu-ūdeņraža pārnešanai (acid–base katalīze) — izmantojot RNS bāzes un 2'-OH;
- metalu jonveida katalīzei — metaljoni stabilizē pārejas stāvokli un aktivizē ūdeņraža atdalīšanos;
- substrātu orientācijai un savienojumu tuvināšanai — samazinot entropisko barjeru.
Veidi un piemēri
Dabiski sastopamie ribozīmi ietver gan mazus, paššķeļošus elementus, gan lielākas RNS vienības ar plašāku funkciju:
- mazie paššķeļošie ribozīmi: hammerhead, hairpin, glmS, twister — bieži sastopami viendzīslu RNS un vīrusu elementu regulācijā;
- HDV (hepatitis delta virus) ribozīms — vīrusu genomā svarīga paššķeļoša aktivitāte;
- grupas I un II introni — lielas ribozīmu struktūras, kas veic samazināšanos (self-splicing) un reizēm piedalās mezas sintezē;
- RNase P — RNP komplekss, kura RNS komponente nodrošina pre-tRNA 5' galvas apstrādi (RNS katalītiska aktivitāte);
- ribosomas peptidiltransferāzes centrs — ribosomālās rRNA katalizē peptīdu saišu veidošanu, kas demonstrē, ka liela RNS molekula var būt galvenais katalizators pat ļoti sarežģītā reakcijā.
Atklāšana un evolūcijas nozīme
1980. gadu sākumā zinātnieki, piemēram, Thomas Cech un Sidney Altman, atklāja, ka RNS spēj veikt katalītiskas funkcijas (piem., T. Cech atklāja pašsplicing-a fenomenu Tetrahymena intronos). Par šīm atklāšanām viņiem piešķīra Nobela prēmiju ķīmijā 1989. gadā. Šīs atziņas būtiski mainīja izpratni par molekulāro biologiju — tās deva pamatu RNS pasaules hipotēzei, kas paredz, ka agrīnajā evolūcijā RNS varēja darboties gan kā ģenētiskā informācijas nesēja, gan kā katalizators, pirms attīstījās proteīnu enzīmi un sarežģīta DNS-replikācija.
Laboratorijā veidoti ribozīmi un polimerāzes
Pētnieki, kas pēta dzīvības rašanos un šūnu evolūciju, laboratoriski izmanto in vitro evolūciju (piem., SELEX, direktēto evolūciju), lai radītu ribozīmus ar jauniem vai uzlabotiem raksturlielumiem. Ir izstrādāti ribozīmi, kas spēj pievienot nukleotīdus, t.i., funkcionēt kā RNS polimerāzes. Piemēram, uzlabotie "Round-18" polimerāzes ribozīma varianti, B6.61 un tC19Z, demonstrēja ievērojamu aktivitāti: "B6.61" 24 stundu laikā var pievienot līdz ~20 nukleotīdiem primertemplī, pirms tas zaudē aktivitāti sašķeļoties; "tC19Z" var pievienot līdz pat ~95 nukleotīdiem ar labu precizitāti. Šie piemēri parāda, ka ribozīmi var darboties kā primitīvas polimerāzes, taču joprojām pastāv ierobežojumi — molekulu stabilitāte, nepieciešamība pēc specifiskiem substrātiem vai katalizatoru apstākļiem (piem., augstas Mg2+ koncentrācijas) un kopējā efektivitāte salīdzinājumā ar proteīnu enzīmiem.
Biomedicīniskās un biotehnoloģiskās pielietošanas
Dažiem ribozīmiem ir potenciāla lietojuma vieta terapijā un biotehnoloģijā. Tie var darboties kā molekulārie "šķērslauži", kas mērķē noteiktas RNS sekvences, tādējādi inhibējot vīrusu replikāciju vai regulējot gēnu ekspresiju. Praktiskie piemēri un iespējas ietver:
- antivielu un antivirālu terapiju izpēti (piem., mēģinājumi mērķēt HIV vai citu vīrusu RNA);
- biosensori — ribozīmi, kas maina aktivitāti vai signālu saistībā ar konkrētu molekulu klātbūtni;
- genomikas rīki un gēnu atklāšana — specifiska RNS šķelšana var palīdzēt mapēt vai nolabīt noteiktas sekvences;
- sintētiskā bioloģija — ribozīmi kā regulējoši elementi mākslīgos RNS tīklos vai kā daļa no pašreplikējošiem sistēmām.
Tomēr klīniskie pielietojumi saskaras ar izaicinājumiem: RNS nestabilitāte organismā, šūnu piegādes problēmas, imūnreakcijas un specifiskuma nodrošināšana. Daudzas no šīm problēmām pēdējos gados risinātas, izmantojot ķīmiskas modifikācijas, vektorus un nanodaļiņas, bet daudzi risinājumi vēl ir attīstības stadijā.
Nākotnes perspektīvas
Ribozīmu izpēte turpina paplašināt mūsu sapratni par molekulāro evolūciju un par iespējamām tehnoloģiskām lietojumprogrammām. Uzlabotas laboratorijas evolūcijas metodes var radīt efektīvākas polimerāžu un katalītiskas aktivitātes, kas palīdz modelēt possible prebiotiskos procesus un attīstīt jaunas biotehnoloģijas. Vienlaikus pētījumi par ribozīmu struktūru un mehānismiem sniedz ieskatu par to, kā RNS varētu darboties kā daudzfunkcionāls molekulārs instruments gan dabā, gan laboratorijā.
Kopumā ribozīmi ir svarīgs bioloģijas laukums, kas savieno fundamentālu pētījumu par dzīvības rašanos ar praktiskām lietojumprogrammām medicīnā un biotehnoloģijā.