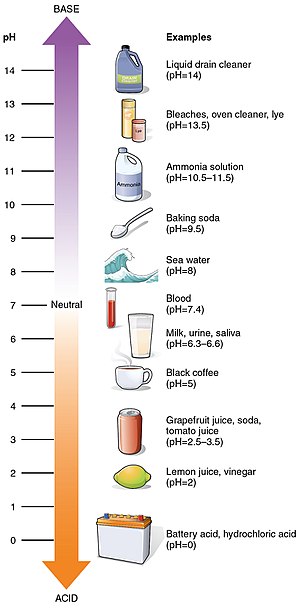
pH ir skābuma skala no 0 līdz 14. Tā norāda, cik skāba vai sārmaina ir viela. Skābākiem šķīdumiem ir zemāks pH. Sārmainākajiem šķīdumiem ir augstāks pH. Vielu, kas nav ne skābas, ne sārmainas (t. i., neitrālu šķīdumu), pH parasti ir 7. Skābēm pH ir mazāks par 7. Sārmu pH ir lielāks par 7.
pH ir protonu (H+) koncentrācijas rādītājs šķīdumā. Šo jēdzienu 1909. gadā ieviesa S.P.L. Sērensens. P apzīmē vācu potenz, kas nozīmē jaudu vai koncentrāciju, un H - ūdeņraža jonu (H+).
Visizplatītākā formula pH aprēķināšanai ir šāda:
pH = - log 10 [ H + ] {\displaystyle {\mbox{pH}}=-\log _{10}\left[{\mbox{H}}}^{+}\right]}
[H+] norāda H+ jonu koncentrāciju (rakstīts arī [H3O+], vienāda hidronija jonu koncentrācija), ko mēra molos litrā (pazīstams arī kā molaritāte).
Tomēr pareizais vienādojums patiesībā ir šāds:
pH = - log 10 [ a H + ] {\displaystyle {\mbox{pH}}}=-\log _{10}\left[a_{\mathrm {H^{+}}} }\right]}
kur a H + {\displaystyle a_{\mathrm {H^{+}} }}} 
Lielākajai daļai vielu pH ir robežās no 0 līdz 14, lai gan ļoti skābām vai sārmainām vielām var būt pH < 0 vai pH > 14.
Sārmainās vielās ūdeņraža jonu vietā ir hidroksīda jonu (OH-) koncentrācija.
Kas nozīmē pH vērtība praktiski
pH skala ir logaritmiska: katrs vienāds pH solis atbilst desmitkārtīgai H+ koncentrācijas izmaiņai. Tas nozīmē, ka šķīdums ar pH 4 satur desmit reizes vairāk H+ jonu nekā šķīdums ar pH 5, un 100 reizes vairāk nekā šķīdums ar pH 6. Tādēļ nelielas pH izmaiņas var būt būtiskas ķīmiskajām un bioloģiskajām sistēmām.
Paraugi ar bieži sastopamām pH vērtībām
- Acetonitrils, ļoti koncentrētas minerālsāls skābes: iespējams pH < 0 (koncentrētas skābes).
- Vēdera skābe (žults/stomaka): apmēram pH 1–2.
- Citronu sula, etiķis: aptuveni pH 2–3.
- Vārīts ūdens / destilēts ūdens ideālā gadījumā: pH ≈ 7 (neitrāls).
- Cilvēka asinis: aptuveni pH 7,35–7,45 (stingri regulēts).
- Jūras ūdens: apmēram pH 8,1 (var mainīties – okeāna acidifikācija).
- Nātrija hidroksīda šķīdums (baltīšana, sārmi): pH 12–14.
Kā pH mēra
- pH-metrs (elektroniskais) — stikla elektrodu sistēma mēra elektrodo potenciālu, kas ir saistīts ar H+ aktivitāti. Lai iegūtu precīzu rezultātu, parasti nepieciešama kalibrācija ar pH standartšķīdumiem.
- Indikatori — organiskas vielas, kuras maina krāsu atkarībā no pH (piem., fenolftaleīns, bromtimols). Noderīgi ātrai aptuvenai novērtēšanai.
- pH papīrs / lakmusa papīrs — krāsu skala, kas salīdzina krāsas maiņu ar standarta tabulu; vienkārši un lēti, bet mazāk precīzi.
Jāatzīmē, ka elektrodu mērījumi reaģē uz jonu aktivitāti, nevis tikai molaritāti — tāpēc koncentrēta šķīduma pH aprēķins tikai pēc [H+] var atšķirties no mērījuma, ja neņem vērā aktivitātes koeficientus.
Bufers un pH stabilitāte
Daudzas sistēmas izmanto buferus, lai saglabātu pH. Bufers satur pāru skābi un tās konjugēto bāzi (piem., acetic acid / acetate). Tas mazina pH maiņu pie pievienota skābes vai bāzes. Bioloģijā ļoti svarīgs piemērs ir asins buferu sistēma, bet arī šūnu reģioni un laboratorijas šķīdumi izmanto buferus.
Vērtīgākās ķīmiskās saiknes
Henderson–Hasselbalch vienādojums saista pH ar pKa un konjugētā pāra koncentrācijām:
pH = pKa + log10([A-]/[HA])
Šo vienādojumu izmanto, lai aprēķinātu bufera darbību un prognozētu pH izmaiņas, kad zināmas skābes un tās bāzes koncentrācijas.
Kāpēc pH ir svarīgs
- Bioloģija: enzīmu aktivitāte un olbaltumvielu struktūra bieži ir atkarīga no pH; nelielas svārstības var ietekmēt šūnu funkcijas.
- Ķīmija: reakciju ātrums, līdzsvara pozīcija un jonizācijas pakāpe ir pH atkarīga.
- Vides zinātne: ūdens ķīmija, notekūdeņu apstrāde, augsnes skābums un okeānu acidifikācija ietekmē ekosistēmas.
- Pārtika un medicīna: pārtikas konservēšana, fermentācija, zāļu formulējumi un cilvēka veselība ir cieši saistīti ar pH.
- Rūpniecība: korozija, ķīmiskās ražošanas procesi un attīrīšana bieži prasa kontrolētu pH līmeni.
Papildu piezīmes par aktivitāti un ekstremālām vērtībām
Reālās šķīdumu ķīmijas aprēķinos bieži lieto jonu aktivitātes (aH+), kas ņem vērā mijiedarbības starp joniem (attiecīgi izmantot aktivitātes koeficientu). Tāpēc precīzs vienādojums nāk ar aktivitāti, ne tikai koncentrāciju — kā tas norādīts augstāk ar attēloto formulu un matemātisko izteicienu.
Dažiem ļoti koncentrētiem šķīdumiem vai situācijām ar stiprām elektrostatiskām mijiedarbībām var novērot pH vērtības, kas ārpus 0–14 robežām (pH < 0 vai pH > 14). Tas nav pretrunā ar definīciju, jo pH tiek definēts kā -log10(no H+ aktivitātes), un aktivitāte var pārsniegt 1.
Kopsavilkums
pH ir fundamentāls rādītājs, kas raksturo šķīdumu skābumu vai sārmainību. To apraksta formulas, kas saista pH ar H+ koncentrāciju vai aktivitāti. Skalas logaritmiskais raksturs nozīmē, ka nelielas pH izmaiņas atbilst lielām H+ koncentrācijas izmaiņām. pH mērījumi un kontrole ir būtiski gan zinātnē, gan rūpniecībā, medicīnā un vides aizsardzībā.
![{\displaystyle {\mbox{pH}}=-\log _{10}\left[{\mbox{H}}^{+}\right]}](https://www.alegsaonline.com/image/093977a79b6a17e02db4699475930e48c05d6468.svg)
![{\displaystyle {\mbox{pH}}=-\log _{10}\left[a_{\mathrm {H^{+}} }\right]}](https://www.alegsaonline.com/image/7a631c4037415f3d4483a6cb07e69858b64890fc.svg)