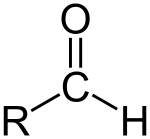
Aldehīds (/ˈældɪhaɪd/) ir organisks savienojums, kas satur formilgrupu. Formilgrupa ir daļa no molekulas ar struktūru R-CHO — to veido oglekļa atoms, kas ir dubultā saitē ar skābekli (C=O) un vienlaikus saistīts ar ūdeņradi un R grupu (R — pārējā molekulas daļa). Grupu bez sānu ķēdes sauc par aldehīdu grupu vai formilgrupu. Aldehīdi atšķiras no ketoniem, jo aldehīdos formilgrupa atrodas molekulas galā (terminali), bet ketonos — molekulas vidū. Aldehīdi ir plaši izplatīti organiskajā ķīmijā, un daudzi aromatiskie savienojumi un smaržvielu komponenti pieder šai grupai.
Struktūra un nomenklatūra
- Vispārīgā formula: R-CHO (R = alkils, aromāts vai H).
- IUPAC nosaukumi parasti beidzas ar galotni "-al" (piem., metanāls = formaldehīds, etanāls = acetaldehīds).
- Bieži sastopami piemēri:
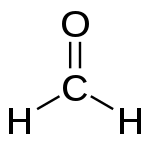
- Formaldehīds (metanāls, H-CHO) — vienkāršākais aldehīds;
- Acetaldehīds (etanāls, CH3-CHO);
- Benzaldehīds (C6H5-CHO) — aromātisks aldehīds ar raksturīgu mandeļu smaržu.
Fizikālās īpašības
- Aldehīdi parasti ir polāri savienojumi (C=O grupa), tāpēc šķīdība ūdenī ir atkarīga no R grupas: mazi aldehīdi (piem., formaldehīds) labi šķīst ūdenī, lielākiem hidrofobiskiem R grupām šķīdība samazinās.
- Zema molekulmasa aldehīdi ir viegli gaistoši un bieži ar asu smaku; aromātiskie aldehīdi ir mazāk gaistoši un var dot patīkamas aromātiskas īpašības.
- Boiling point tradicionāli ir augstāks nekā atbilstošam alkānam, bet zemāks nekā karboksilskābēm ar līdzīgu masas.
Klīniskās un kemiskās īpašības (reakcijas)
- Aldehīda oglekļa atoms ir elektrofīlis — tas viegli piedalās nukleofilās pievienošanās reakcijās (piem., hidrāta veidošanās, cianhidrīna pievienošanās).
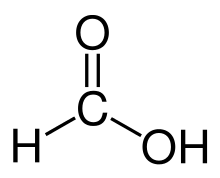
- Oksidācija: aldehīdi viegli oksidējas līdz atbilstošajām karboksilskābēm (piem., acetaldehīds → pienskābe). Šī īpašība ļauj atšķirt aldehīdus no ketoniem ar oksidējošiem reaģentiem.
- Redukcija: aldehīdus var reducēt uz primārajiem alkoholiem (piem., ar NaBH4 vai katalītisku hidrogenēšanu).
- Kondensācijas un alfa-reakcijas: ja aldehīdam ir α-hidrogrupas, var notikt enolizācija un aldolreakcijas (aldol kondensācija). Bez α‑hidrogēna aldehīdi var piedalīties Cannizzaro reakcijā (disproporcionēšanās) stipri bāziskos apstākļos.
- Specifiski testi: Tollena (sudraba spogulis) un Fehlinga reaģenti oksidē aldehīdus, radot atbilstošas pozitīvas reakcijas; Šīfa reagens arī atklāj aldehīdus.
- Polimerizācija un adīcijas: daži aldehīdi (īpaši formaldehīds) polimerizējas vai veido reaktīvas adukcijas, ko izmanto rēzusos un sveķos.
Sintezes metodes
- Primāro alkoholu selektīva oksidācija (piem., PCC, Swern, TEMPO katalīze) — plaši izmantota aldehīdu iegūšanai.
- Rosenmund reducēšana — acilhlorīdu reducēšana uz aldehīdiem, kontrolējot tālāko redukciju.
- Hydroformilācija (oxo reakcija) — alkēnu reakcija ar CO un H2, lai iegūtu aldehīdus (piemērā cetil- vai linearas aldehīdu ražošana industriāli).
- Vilsmeiera–Haack reakcija — aromātisku slāpekļa saturošu savienojumu formilēšana.
- Gattermann–Koch reakcija — benzola atvasinājumu formilēšana (piem., benzaldehīda syntēze no benzola).
- Ozonolīze — alkēnu selektīva šķelšana var dot aldehīdus atkarībā no darba apstrādes (kontrolējot reducējošu vai oksidējošu pēcapstrādi).
Spektroskopiskas pazīmes
- IR spektroskopijā raksturīgs C=O šūpojums aptuveni 1720–1740 cm−1 (konjugācijā vai aromātiskos gadījumos frekvence samazinās).
- 1H NMR: aldehīdprotons parasti parādās ap 9–10 ppm kā nosacīti spilgta signals.
- 13C NMR: karbonilreaktīvā C-atoma signals parasti starp 190–205 ppm.
Pielietojumi
- Formaldehīds — svarīga izejviela sveķu, polimēru (urea‑formaldehīds, fenol‑formaldehīds), dezinfekcijas līdzekļu un konservantu ražošanā.
- Benzaldehīds — aromatizētājos un smaržvielu komponentēs (mandeļu smarža).
- Aldehīdi kopumā — starpprodukti farmaceitiskajā industrijā, agroķīmijā, krāsu un pigmentu sintēzē, smaržvielu un pārtikas aromatizētāju ražošanā.
- Industriāli izmanto aldehīdu reaktivitāti, lai izveidotu polimērus, preparātu atvasinājumus un kondensācijas produktus.
Drošība un ilgtspēja
- Daudzi aldehīdi ir kairinoši acu un elpceļu gļotādām; zemā molekulmasa aldehīdi bieži ir toksiski un gaistoši.
- Formaldehīds ir klasificēts kā kancerogēns cilvēkam (IARC) un prasa īpašu piesardzību — ventilācija, aizsargaprīkojums un atbilstoša darba drošība.
- Ar aldehīdiem strādājot, jāievēro atbilstoši drošības datu lapu norādījumi (SDS) un apkārtējās vides aizsardzības prasības.
Kopsavilkumā, aldehīdi ir svarīga organiskās ķīmijas grupa ar raksturīgu formilgrupu R-CHO, plašu reakciju spektru un nozīmīgiem pielietojumiem rūpniecībā, farmācijā un smaržu ražošanā, taču tie prasa uzmanīgu rīkošanos tieši to toksicitātes un reaktivitātes dēļ.