Šis raksts ir tikai par spirtu ķīmiju.
Dzērienos izmantotais alkohols ir etanols; vairāk informācijas var atrast vietnē alkoholiskie dzērieni un alkoholisms.
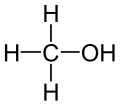
Ķīmijā alkohols ir vispārīgs termins, kas apzīmē daudzus organiskos savienojumus, kurus izmanto rūpniecībā un zinātnē kā reaģentus, šķīdinātājus un degvielu. Alkoholi ir ogļhidrāti, kas sastāv no alkilgrupas ar vienu vai vairākām hidroksilgrupām (-OH), kas saistītas ar oglekļa atomiem. Alkohols ir bezkrāsains un caurspīdīgs.
Kopējā definīcija un korekcija
Ķīmiskajā kontekstā alkoholi ir organiskie savienojumi, kuros vienam vai vairākiem oglekļa atomiem ir saistīta hidroksilgrupa (-OH). Svarīgi precizēt, ka alkoholi nav tas pats, kas ogļhidrāti — ogļhidrāti (karbohidrāti) ir cita molekulu klase. Iepriekš minētā saite uz "ogļhidrāti" atrodama sākotnējā tekstā, taču jāuzsver, ka alkoholi ir plašāka organisko savienojumu grupa, kuras piemēri ietver metanolu, etanolu, propanolu, izopropanolu, butanolu, glicerīnu u.c.
Klasifikācija
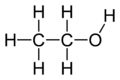
- Pirmējie (primārie) alkoholi: hidroksilgrupa pie oglekļa, kas saistīts ar vienu citu oglekļa atomu (piemērs: etanols, CH3CH2OH).
- Otrējie (sekundārie) alkoholi: hidroksilgrupa pie oglekļa, kas saistīts ar diviem citiem oglekļa atomiem (piemērs: izopropanols).
- Trešējie (teriārie) alkoholi: hidroksilgrupa pie oglekļa, kas saistīts ar trim oglekļa atomiem (piemērs: terc-butanols).
- Polioli (daudzvērtīgie alkoholi): satur vairākas -OH grupas, piemēram, glikolus (etilēnglikols), glicerīnu (glicerols).
- Aromātiskie alkoholi: hidroksilgrupa pie aromātiska cikla (piemērs: benzilspirts). Fenoli (piem., fenols) ir saistīti ar aromātisko ciklu, taču to īpašības (piem. skābums) atšķir tos no parastajiem alkoholiem.
Fizikālās īpašības
- Vispārīgi bezkrāsaini šķidrumi (gāzveida vai cietas formas iespējamas atkarībā no molekulmasas).
- Hidroksilgrupa nodrošina ūdeņūdeņu saišu veidošanos starp molekulām, tāpēc alkoholi bieži ir viskozi, tiem ir augstāki kušanas un viršanas punkti nekā atbilstošiem hidrokarboni.
- Polaritāte: mazās ķēdes alkoholi (piem., metanols, etanols) ir labi šķīstoši ūdenī; ar garāku alkilķēdi solubilitate ūdenī samazinās.
- Degamība: daudzi šķidrie alkoholi ir viegli uzliesmojoši (piem., etanols, metanols, izopropanols).
Ķīmiskās īpašības un būtiskākās reakcijas
- Skābuma/bāziskuma īpašības: alkoholi ir vāji skābi (pKa ~15–19 atkarībā no struktūras). Parasti tie rīkojas kā vāji skābi protoli, bet spēcīgāku bāzu klātbūtnē var deprotonēties, veidojot alkoksīdjonus (R–O−).
- Oksidācija: primārie alkoholi var oksidēties līdz aldehīdiem un tālāk līdz karbonskābēm; sekundārie — uz ketoniem; terciārie parasti neoksidējas viegli bez ķēmiski agresīvākiem apstākļiem.
- Esterifikācija: alkoholi reaģē ar karbonskābēm, veidojot esterus (piem., etanols + etiķskābe → etilacetāts + ūdens) parasti skābes katalizēta.
- Dehidratācija: siltuma un katalizatora (piem., svina sulfrāts, sērsskābe) iedarbībā alkoholi var dehidrēties, veidojot alkenus.
- Substitūcijas: -OH grupa var tikt aizstāta ar halogēniem vai citām grupām, izmantojot piemērotus reaģentus (tosilēšana, halogenēšana).
Ražošanas galvenās metodes
- Fermentācija: etanols komerciālajā tirdzniecībā tiek iegūts, fermentējot cukurus ar raugiem (biotehnoloģisks process, izmanto pārtikas rūpniecībā un degvielā).
- Hidratācija (alkēnu pievienošana ūdenim): alkēnu katalītiska hidratācija sniedz dažādus alkoholus rūpnieciskā mērogā (piem., etilēna hidratācija līdz etanolam).
- Sintētiskā ķīmija: reducēšana (aldehīdu/ketonu reducēšana), halogenētu savienojumu reakcijas ar hidroksīdu u.c.
- Speciālie polioli (piem., glicerīns) bieži iegūst kā blakusproduktu no tauku hidrolīzes vai biodīzeļražošanas.
Pielietojums
- Ketiliskos un laboratorijas šķīdinātājos (etanols, izopropanols).
- Degvielas un degvielas piedevas (etanols kā biodegviela, metanolam rūpnieciska nozīme kā sintēzes izejvielai).
- Antiseptiķi un dezinfekcijas līdzekļi (etanols, izopropanols).
- Rūpnieciskie izejmateriāli: plastmasu, šķīdinātāju, augšējo reakciju reaģentu ražošanā, kā arī farmācijā un kosmētikā.
- Skābekļa pārnese un antifrīzi: etilēnglikols (antifrīzs), propilēnglikols pārtikas un farmācijas rūpniecībā.
- Pārtikas un dzērienu ražošana: etanols alkoholiskajos dzērienos (par to lasāms zem saites "etanols" un "alkoholiskie dzērieni").
Drošība un toksicitāte
- Metanols (metilspirts) ir ļoti toksisks — pat nelielas devas var izraisīt aklumu vai nāvi, jo organisms to metabolizē formiāta un formaldehīda toksiķos produktos.
- Etanols (dzērienu spirts) rīkojas kā centrālās nervu sistēmas nomācošs līdzeklis; pārmērīga lietošana izraisa intoksikāciju, atkarību un hroniskas veselības problēmas.
- Daudzi šķidrie alkoholi ir uzliesmojoši — jāievēro ugunsdrošības prasības.
- Darbs ar koncentrētiem šķīdumiem prasa ventilāciju, personīgās aizsardzības līdzekļus (cimdi, acu aizsardzība).
Praktiski piemēri
- Metanols (CH3OH) — rūpniecībā, taču ļoti toksisks.
- Etanols (CH3CH2OH) — dzērienos, kā šķīdinātājs un degviela.
- Izopropanols (izopropilsprits) — dezinfekcijā un tīrīšanā.
- Etilēnglikols — antifrīzs; propilēnglikols — mazāk toksisks polials, lieto pārtikā un farmācijā.
- Glicerīns (glicerols) — trīsvērtīgs alkohols, mitrinātājs un farmācijas izejmateriāls.
Svarīgākie punkti — kopsavilkums
Alkoholi ir plaša organisko savienojumu klase ar hidroksilgrupu (-OH). Tie ir svarīgi rūpniecībā, laboratorijās un ikdienā — no dzērienu etanola līdz technoloģiskajiem šķīdinātājiem un antifrīziem. Lai gan daudzi alkoholi šķiet līdzīgi, to ķīmiskās īpašības, toksicitāte un pielietojumi ļoti atšķiras, tāpēc nepieciešama uzmanība gan lietošanā, gan uzglabāšanā.