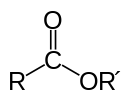
Esteris ir karbonils ar ētera grupu oglekļa atomā. Šo grupu var rakstīt kā COOR. Tos var izgatavot, reaģējot karboksilskābei ar alkoholu ar kādu skābi.
Esteri ir ļoti svarīga funkcionālā grupa. Tos var atrast daudzās vielās. Tie ir ļoti bieži sastopami taukos un eļļās. Dažreiz tiem ir ļoti spēcīga, patīkama smarža. Tos var izmantot smaržu izgatavošanai. Poliesteri ir sastopami plastmasās.
Arī esteri var veikt daudzas reakcijas. Molekulas ētera daļu ir ļoti viegli nomainīt pret citu līdzīgu. Esteri var arī reducēt līdz ketonam vai alkoholam, ar ko var veikt daudzas dažādas reakcijas. Nukleofīlā pievienošana arī ir laba reakcija, lai gan nedaudz sarežģītāka nekā ar ketoniem.
Ir vairāki veidi, kā noskaidrot, vai molekulai ir estera grupa. Infrasarkanā spektroskopija dod ļoti asus signālus, kas atšķiras no citiem karboniliem. Oglekļa NMR spektroskopijai ir līdzīgas īpašības.
Struktūra un nomenklatūra
Esterim vispārējā formula ir R–COO–R', kur R un R' var būt alkilgrupas vai organiskas atlikas. Karbonilskābes oglekļa atoms (C=O) ir savienots ar skābekļa atomu, kurš tālāk saistīts ar R' grupu. Starp esteru un citu karbonilsaturu (piem., aldehīdiem, ketoniem vai amīdiem) esteri izceļas ar oksigēna saiti, kas rada īpašas ķīmiskās īpašības.
Nomenklatūrā lieto nosaukumus, kuri parasti sastāv no alkilgrupas nosaukuma (no R') un karboksilskābes atvasinājuma nosaukuma (piem., etilacetāts = etil etanoaāts).
Fizikālās īpašības
- Polarizācija: Esteriem ir polāra C=O saite, bet tie nav ūdeņraža donorķīmiskas (nav OH grupas), tāpēc ūdens šķīdība ir ierobežota atkarībā no ķēdes garuma.
- Vārīšanās temperatūra: Parasti zemāka nekā attiecīgiem alkoholiem vai karboksilskābēm ar līdzīgu molekulmasu, jo trūkst stipru ūdeņraža saišu starp molekulām.
- Smaka: Daudzi esteri ir aromātiski un tiek izmantoti aromatizatoros un smaržās (piem., etilbutirāts smaržo pēc ananasa).
- Bioloģiskā nozīme: Tauki un eļļas ir triglicerīdi — esteri, kuros glikolītis (glicerols) ir esterificēts ar taukskābēm.
Galvenās ķīmiskās reakcijas
- Hidrolyze: Esteri viegli hidrolizējas skābē vai sārmos. Sārmainā hidrolīzē (saponifikācijā) veidojas karboksilāta sāls un alkohols — tas ir ziepju ražošanas pamats.
- Transesterifikācija: Alkohola apmaiņa starp esteriem un alkoholiem; būtiski polimēru (poliesteru) sintēzē un biodegradācijā.
- Aminolīze: Esteri reaģē ar amīniem, veidojot amīdus.
- Redukcijas: Spēcīgi reducētāji, piemēram, LiAlH4, reducē esterus līdz primārajiem alkoholam. Selektīvas reducēšanas (piem., DIBAL-H pie zemas temperatūras) var apturēt procesus pie aldehīda stadijas.
- Nukleofilā pievienošanās/atrašanās: Nukleofīli var atakēt karbonilskābes oglekli, kas novērš estera grupu un rada dažādus produktus atkarībā no nukleofīla.
Sintēze
Visizplatītākā metode ir esterifikācija — reaģējot karboksilskābei ar alkoholu ar kādu skābi kā katalizatoru (Fischer esterifikācija). Citi parasti izmantotie ceļi ir reagēšana ar acilhlorīdiem vai anhidrīdiem, metilēšanas/transesterifikācijas metodes rūpnieciskā mērogā, kā arī enzimātiskas esterifikācijas biotehnoloģijā.
Identifikācija un analītiskās metodes
- Infrasarkanā (IR) spektroskopija: Raksturīgs C=O stretching apmēram 1735–1750 cm−1 alifātiskiem esteriem; konjugācija vai aromātiskums šo frekvenci samazinās.
- NMR spektroskopija: 1H NMR rāda alkilgrupu signālus; 13C NMR karbonilogleklim parasti ap 160–185 ppm.
- MS un GC–MS: Ļauj noteikt molekulmasu un fragmentācijas shēmas, noderīgi aromātu un šķīdinātāju analīzē.
- TLC un HPLC: Lietojami atdalīšanai un kvantitatīvai analīzei kompozītos maisījumos.
Pielietojums
- Rūpnieciskie šķīdinātāji (piem., etilacetāts), ekstrakcijas līdzekļi.
- Smaku un garšu piedevas pārtikā un kosmētikā (dabīgi un sintētiski esteri).
- Plastmasas un šķiedras — poliesteri (piem., PET) tiek iegūti no diola un dikarboksilskābju esteriem.
- Plastifikatori un farmaceitiskie starpprodukti.
- Bioloģiski — triglicerīdi taukos un eļļās ir esteri, kuru hidrolīze ir būtiska metabolismā.
Drošība un vide
Daudzi esteri ir viegli uzliesmojoši šķīdinātāji un jālieto ar ventilāciju un atbilstošu individuālo aizsardzību. Dažas estera atvasinājumu grupas (piem., noteikti ftalātu esteri) var būt vides vai veselības riska faktori (hormonu sistēmas traucējumi). Svarīgi ievērot materiālu drošības datnes (MSDS) un vietējos noteikumus par uzglabāšanu un iznīcināšanu.
Piemēri
- Etānaāts (etiķskābes etilesters) — etilacetāts: plaši lietots šķīdinātājs, raksturīga augļu smarža.
- Propānaāts, metilpropionāts: aromatizatori pārtikā.
- Triglicerīdi: dabīgie tauki un eļļas, piemērs esteriem bioloģiskā kontekstā.
Šī apkopojuma mērķis ir sniegt pārskatu par esteriem — to struktūru, īpašībām, reakcijām, analīzes metodēm un pielietojumu ikdienā un rūpniecībā.