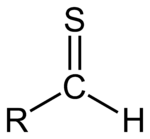
Tials jeb tioaldehīds ir jebkura molekula ar grupu RC(S)H. Strukturāli tas atgādina parastu aldehīdu, kurā aldehīda skābekļa atoms ir aizstāts ar sēra atomu. Sēram veidojas dubultā saite ar oglekli, un tas saglabā divus vientuļos pārus, kas ietekmē molekulas elektronisko blīvumu un reaktivitāti.
Īpašības
Tiali parasti ir ļoti reaktīvas un bieži šķiet elektrofili — tioaldehīda karbonilgrupa (C=S) pievelk elektronus un veicina nukleofilas pievienošanās reakcijas. Salīdzinot ar parastajiem aldehīdiem, C=S saišu π-orbitāļu pārklāšanās ir vājāka nekā C=O, tāpēc tioaldehīdi bieži ir vēl reaģētspējīgāki. No fizikālajiem raksturlielumiem tiem mēdz būt raksturīga intensīva—bieži nepatīkama—smaka.
Reaktivitāte un tipiskās reakcijas
Tāli viegli reaģē ar sevi un ar citiem reaģentiem. Biežākie reakciju veidi:
- Nukleofilas pievienošanās pie C=S, kas rada tiohemiacetālu vai tioacetālu starpproduktus.
- Polimerizācija vai dimerizācija — daudz tioaldehīdu ātri oligomerizējas vai kondensē viena ar otru, tādēļ tos grūti saglabāt izolētā formā.
- Dilsa–Aldera reakcijas un citas [4+2] cikloadīcijas — tioaldehīdi ir labi dienofīli un var veidot cikliskus produktus ļoti ātri.
- Fotokemiskas vai termiskas [2+2] pievienošanās un citi cikloķīmijas ceļi atkarībā no nosacījumiem.
Lielākā reaktivitāte padara tioaldehīdus noderīgus sintēzē kā īslaicīgus starpproduktus, tomēr prasa īpašu piesardzību, lai novērstu nevēlamas blakusreakcijas.
Sintēze un stabilitāte
Parastā pieeja tioaldehīdu iegūšanai ir esoša aldehīda tiacināšana — skābekļa aizstāšana ar sēru, izmantojot tādus tiacionošanas reaģentus kā Lawessona reaģents vai P4S10 (fosfora pentasulfīds). Reakciju nosacījumi parasti ir maigāki un tiek veikti inertā atmosfērā, jo produktu var ātri bojāt vai tas var reaģēt tālāk.
Tioaldehīdu stabilitāte ievērojami palielinās, ja R grupa ir steriski apjomīga (piem., lieli alkil- vai aromātiskie substituenti) vai elektroniski stabilizējoša. Tāpat tioaldehīdi ar konjugētiem aromātiskiem R grupām bieži ir mazāk reaktīvi nekā vienkārši primārie tioaldehīdi. Ja aldehīda H atoms tiek aizstāts ar citu R grupu, produktam piešķir nosaukumu tioketons, kuri parasti ir relatīvi stabilāki nekā tioaldehīdi.
Spektroskopiskas pazīmes
Tioaldehīdi atšķiras no aldehīdiem arī spektroskopiski — C=S grupa dod raksturīgas vibrācijas IR spektrā un bieži izpaužas arī UV–Vis apertūrās saistībā ar n→π* pārejām. NMR spektri parāda atšķirīgas ķīmiskās pārvietojuma vērtības tio- oglekļiem, tomēr konkrētas vērtības atkarīgas no substituentiem un molekulas vides.
Pielietojums un drošība
Tioaldehīdus izmanto organiskajā sintēzē kā reaktīvus starpproduktus ciklookārbu iegūšanai, heterociklu veidošanai un citas specifiskās pievienošanās reakcijās. Tomēr jāievēro piesardzība: daudzi tioaldehīdi ir smaržīgi, var būt toksiski un reaģēt intensīvi ar gaisu vai mitrumu. Strādājot ar tiem, ieteicams izmantot inertu atmosfēru (argons/slāpeklis), zemākas temperatūras un atbilstošus individuālās aizsardzības līdzekļus.
Kopsavilkumā: tials ir sēru saturošs analogs aldehīdam ar augstu reaktivitāti un īpatnējiem ķīmiskajiem un fizikālajiem raksturlielumiem. To praktiska izmantošana sintēzē prasa rūpīgu nosacījumu kontroli un bieži stabilizējošas stratēģijas (piem., steriskā aizsardzība).