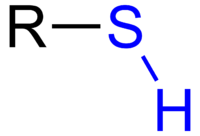
Tiols ir molekula ar R-SH grupu. Tioli ir tādi paši kā spirti, kuros skābekļa atoms ir nomainīts ar sēra atomu. Tiem bieži ir ļoti spēcīga un nepatīkama smaka. Tiolus pievieno dabasgāzei, lai cilvēki varētu sajust to smaržu. Tas ir tāpēc, ka metānam nav smakas, bet tas var viegli eksplodēt.
Tioli ļoti viegli oksidējas. Tie ir arī diezgan skābi, vairāk nekā spirti. Ja protonu atņem bāze, tiols var kļūt par nukleofilu. Tas var veikt tādas reakcijas kā nukleofīlā aizvietošana.
Viena no dabiskajām aminoskābēm - cisteīns - savā struktūrā satur tiolu.
Kas ir merkaptāni un nosaukuma izcelsme
Tiolus bieži sauc arī par merkaptāniem. Nosaukums cēlies no latīņu saknes, kas saistīta ar spēju veidot stipras saites ar dzīvsudrabu (mercurium captans — 'ķer dzīvsudrabu'). Termins norāda uz sēra grupas lielo afinitāti pret dažiem metāliem.
Fizikālās un ķīmiskās īpašības
- Formāla struktūra: R–SH, kur R var būt alkil-, aril- vai cita organiskā grupa.
- Smarža: daudzi tioli ir ļoti smaržīgi un bieži raksturoti kā sēru, atkritumu vai “rūgtu” smaku. Smaržas slieksnis ir ļoti zems — daži tioli jūtami ļoti zemās koncentrācijās (ppb–ppm līmenī), tāpēc tos izmanto kā gāzes aromatizētājus.
- Skābība: tioli ir skābāki nekā atbilstošie spirti; tiolu pKa parasti ir aptuveni 8–12, kamēr spirtu pKa parasti ir ~16–18. Tāpēc tie vieglāk deprotonējas un veido thiolātu anjonu (RS−).
- Reaktivitāte: thiolāts (RS−) ir labs nukleofils un reducētājs. Tioli viegli oksidējas līdz disulfīdiem (R–S–S–R) un var tālāk oksidēties līdz sulfonātiem vai sulfoniem atkarībā no apstākļiem.
- Saistīšanās ar metāliem: Sēra atoms labi koordinējas ar daudziem metāliem, tāpēc tioli veido stabilas kompleksvielas un tiek izmantoti kā ligandi koordinācijas ķīmijā.
Galvenās ķīmiskās reakcijas
- Oxidācija: divi tioli oksidējoties veido disulfīdu (R–S–S–R). Šī reakcija ir svarīga bioloģiski (disulfīdu tilti proteīnos) un sintētiski.
- Deprotonācija: bāzes klātbūtnē tiols atdala H+ un veido thiolātu (RS−), kas ir aktīvs nukleofils. Tas ļauj veikt S-alkilāciju un citas S-aizvietošanas reakcijas.
- Thiol–ene reakcijas: ātras "klik" tipa pievienošanās reakcijas starp tioliem un alkēniem, plaši izmantotas materiālu ķīmijā.
- Veidošanās un šķelšanās disulfīdiem: svarīga redoksreakcija proteīnu strukturālai stabilitātei un daudzās sintētiskajās procedūrās.
Bioloģiskā loma
Tiolu grupa cisteīnā ir kritiska proteīnu struktūras un funkciju nodrošināšanai. Divu cisteīnu tiolu oksidācija veido disulfīdu tiltu (cistīnu), kas stabilizē proteīnu trešējās struktūras vai starp ķēdēm veido saites, ietekmējot enzymu aktivitāti, receptoru funkcijas un šūnu signālu pārvadi.
Pielietojumi
- Dabasgāzes aromatizācija: lai dabasgāze būtu cilvēka deguna jūtama (gāzei piemīt bezkrāsaina un bezsmaržas īpašība), tai pievieno ļoti smaržīgus tiolus (piemēram, etāntiolus, tert-butiltiolus).
- Organiskā sintēze: tioli darbojas kā reagenti un starpprodukti: katalizatori, aizsarggrupas, nukleofili S-alkilācijai un citām transformācijām.
- Medikamenti un bioķīmija: daudzām farmakoloģiski aktīvām molekulām ir sēra saturošas grupas; tiolu reaktivitāte tiek izmantota biokonjugācijai un zāļu dizainā.
- Virsmu modificēšana: cisteinām līdzīgas tiolu grupas cieši saistās ar zelta virsmām — to izmanto self-assembled monolayers (SAM) veidošanā nanotehnoloģijās un biosensoros.
- Piemares aromāti un pārtikas ķīmija: nelielos daudzumos daži tioli piešķir patīkamas aromātiskas īpašības (piemēram, dažos vīnos un kafijā identifikēti tioli, kas dod "augļainu" vai "tropeisku" aromātu).
- Metālu attīrīšana un vīšanu: sēra afinitāte pret smagajiem metāliem ļauj tiolus izmantot attīrīšanas metožu un ekstrakciju procesos.
Drošība un apkarošana
Tioli ir viegli uzliesmojoši un bieži ļoti nepatīkami smaržo; daži ir toksiski vai kairinoši elpceļiem. Darbojoties ar tioliem, ieteicams:
- strādāt labi vēdināmās telpās vai atsevišķā instrumentētā skapī (fume hood);
- lieto personīgās aizsardzības līdzekļus — cimdus un aizsargbrilles;
- uzglabāt cieši noslēgtos konteineros, lai ierobežotu izgarojumu izplatīšanos;
- ja nepieciešams, izmantot absorbentus vai ķīmiskos dezodorantus smakas neutralizēšanai rūpnieciskās iekārtās.
Analītiskās metodes
Tiolu klātbūtni un koncentrāciju nosaka, izmantojot dažādas metodes: plūsmas ķromatogrāfija ar detektoru, gāzu hromatogrāfija–masu spektrometrija (GC–MS), FTIR un NMR spektroskopija, kā arī speciāli sensoru materiāli, kas reaģē uz sēra savienojumiem. Smakas detektēšanai praktiski izmanto arī cilvēka degunu kā jutīgu indikatoru, taču tas nav drošs kontrolēšanai bīstamības apstākļos.
Kopumā tioli (merkaptāni) ir ķīmiskas vielas ar izteiktu un plašu reaktivitāti, nozīmīgu lomu gan bioloģijā, gan rūpniecībā — no gāzes drošības nodrošināšanas līdz molekulārām konstrukcijām un materiālu izstrādēm.