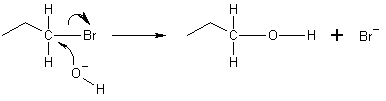
Nukleofils ir suga, kas reakcijas laikā nodod elektronu pāri elektrofilam, lai veidotu ķīmisko saiti. Visas molekulas vai joni ar brīvu elektronu pāri var būt nukleofili. Šo elektronu pāri sauc par vientuļo pāri. Tā kā nukleofili ziedo elektronus, tie atbilst Luisa bāzu definīcijai.
Kas ir nukleofilitāte un nukleofīlais raksturs
Nukleofīlais raksturo nukleofila piesaisti kodoliem. Nukleofilitāte, dažkārt saukta par nukleofila spēku, attiecas uz vielas spēju dāvināt elektronus un reaģēt ar elektrofilu. Tā ir praktiska īpašība, ko izmanto, lai salīdzinātu, kurš reagents noteiktos apstākļos reaģēs ātrāk vai efektīvāk.
Faktori, kas ietekmē nukleofilitāti
- Elektroniskā lādē: parasti negatīvi lādēti atomi/joni (piem., OH−, CN−) ir labāki nukleofili nekā to neitrālie analogi (piem., H2O, HCN).
- Atoms vai grupas polarizējamība: lielāki, vieglāk polarizējami anjoni (piem., I−) var būt stipri nukleofili aprotiskos šķīdinātājos, jo tie viegli izveido pārejas stāvokli.
- Steriskā aizsardzība: apjomīgas substitūcijas ap reaktīvo centru samazina nukleofilu piekļuvi un samazina reaktivitāti.
- Elektronu pievilkšana (elektronegatīvums): vairāk elektronegatīvi atomi notur elektronus ciešāk un parasti ir sliktāki nukleofili.
- Solvēta ietekme: protiski un aprotiski šķīdinātāji atšķirīgi ietekmē jonu stabilitāti un tādējādi nukleofilitāti.
Solvēta ietekme — protiski pret aprotiskiem šķīdinātājiem
Solvents ievērojami maina, kurš nukleofils ir «spēcīgāks». Protoski šķīdinātāji (piem., alkoholi, ūdens) var saistaies ar negatīviem joniem, apvalkot tos ar ūdeņraža saites, kas samazina to reaktivitāti. Tāpēc protiskos šķīdinātājos mazie, stipri hidratēti anjoni (piem., F−) parasti ir vājāki nukleofili nekā lielāki, mazāk hidratēti anjoni (piem., I−). Aprotiskos šķīdinātājos (piem., DMSO, acetons) šādas hidratācijas nav, un mazāki, vairāk elektronegativitāti saturējoši anjoni var būt labāki nukleofili (piem., F− bieži ir spēcīgāks nekā I− aprotiskā šķīdinātājā).
Nukleofilās reakcijas — galvenie tipi un mehānismi
- Nukleofilā aizvietošana (SN): bieži sastopamas divas pamatmehānikas:
- SN2 — vienpakāpju mehānisms, kur nukleofils tieši uzbrūk oglekļa centram, izspiežot atstāšanas grupu; raksturīgs labam nukleofilam, mazam steriskajam apgrūtinājumam un labam atstāšanas grupas spēkam.
- SN1 — divpakāpju mehānisms, kur vispirms veidojas karbokations (atstāšanas grupas atslēgšanās), pēc tam to pievieno nukleofils; reakciju ātrumu nosaka karbokationa veidošanās, tāpēc šādos gadījumos nukleofils mazāk ietekmē ātrumu.
- Adīcija pie karbonilgrupām: nukleofili (piem., RO−, R2N−) var pievienoties aldehīdiem un ketoniem, veidojot alkoksīdus vai hemiacetālus.
- Epoksīdu atvēršana: nukleofili atver epoksīdu gredzenu, bieži ar reģioselektivitāti, kas nosaka, kurš ogleklis tiek uzbrukts (skābes vai bāzes katalizētos apstākļos dažādas prefereneces).
- Nukleofilā aromātiskā aizvietošana (SNAr): aromātisku sistēmu aizvietošana ar nukleofilu, ja ir spēcīgs atstāšanas grupas stabilizējošs elements un elektronatņemjošas substitūcijas.
Nukleofili pret bāzēm — galvenās atšķirības
Lai gan nukleofili bieži ir arī bāzes (abi dāvā elektronus), starp šīm īpašībām ir svarīgas atšķirības:
- Bāze reaģē ar protoniem (H+) — tās spēju mēra pēc protolītiskās jūtības (piem., pKa); bāziskums raksturo stabilitāti veidotajam H‑saturētajam produktam.
- Nukleofils reaģē ar elektronu trūkstošiem centriem (elektrofiliem); nukleofilitāte vairāk atkarīga no reaktīvas pārejas stāvokļa un solventa apstākļiem nekā bāziskums.
- Dažreiz viela var būt laba nukleofila, bet vāja bāze (piem., I−), vai otrādi — laba bāze, bet vāja nukleofila sterisku apstākļu dēļ (piem., t‑BuO−).
Bieži izmantotie nukleofili — piemēri
- Anjoni: OH−, OR− (alkoksi), CN−, N3−, halīdi (Cl−, Br−, I−)
- Neitrālas molekulas: NH3, H2O, alkoholi (piemēram, MeOH) — nereti lēnākas nekā to anjoniskie ekvivalenti, bet joprojām reaģē ar atbilstošiem elektrofiļiem.
- Organometāliski nukleofili: Grignarda reaktīvi (RMgX), organolitija savienojumi (RLi) — ļoti spēcīgi nukleofili, kas reaģē ar karboniliem un citām funkcionālajām grupām.
Praktiski padomi laboratorijā
- Izvēloties nukleofilu, ņem vērā šķīdinātāju — protiski šķīdinātāji mēdz mazināt anjonu reaktivitāti.
- Stipri steriski apgrūtināti nukleofili (piem., t‑BuO−) bieži veicina eliminācijas reakcijas (E2) vairāk nekā aizvietošanu (SN2).
- Atstāšanas grupas spēks (piem., tosāta vai halogenīdi) būtiski ietekmē aizvietošanas reakciju tehoktivitāti — labas atstāšanas grupas (stabilas bāzes) veicina SN1/SN2 reakcijas.
Kopsavilkumā, nukleofils ir viela, kas nodod elektronus elektrofilam, veidojot ķīmiskas saites; nukleofilitāte ir daudzfaktoru īpašība, ko ietekmē lādējums, polarizējamība, steriskie apstākļi un solvents. Saprašana par šiem faktoriem palīdz paredzēt un plānot organiskās reakcijas, it īpaši nukleofilās aizvietošanas un adīcijas procesus.