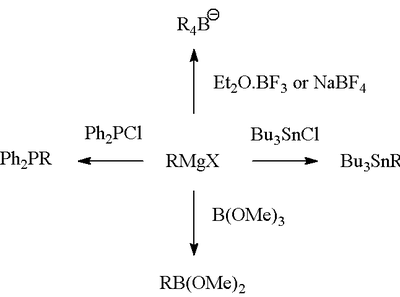
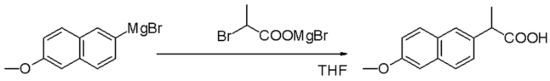
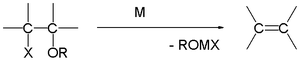
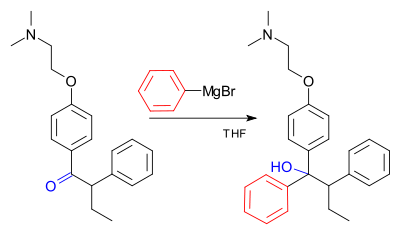
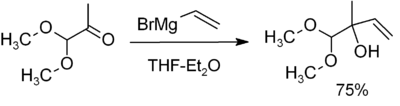Grignarda reakcija (izrunā /ɡriɲar/) ir metālorganiska ķīmiska reakcija, kurā alkil‑ vai aril‑magnija halogenīdi (Grignarda reaģenti, parasti apzīmēti kā R–MgX) uzbrūk elektrofīlajiem oglekļa atomiem polārajās grupās, piemēram, karbonilos. Grignarda reaģenti darbojas kā spēcīgi nukleofili un bāzes ar nozīmīgu karbanjonu raksturu pie oglekļa‑magnija saišu, tādējādi ļaujot veidot jaunas oglekļa–oglekļa saites. Reakcijas rezultātā veidojas metālalkoksīdu starpprodukti, kuri pēc skābas apstrādes (workup) dod atbilstošos alkoholu, karbonskābju vai citus produktus. Grignarda reaakcijas var izmantot arī, lai izveidotu oglekļa–fosfora, oglekļa–alvas, oglekļa–silīcija, oglekļa–bora un citas oglekļa‑heteroatomu saites.
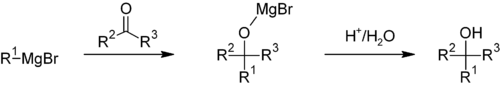
Reakcijas mehānisms
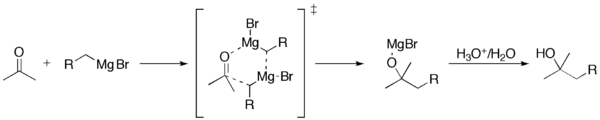
Parasti Grignarda reakcijas mehānisms ietver šādas pamatfāzes:
- Veidojas Grignarda reaģents R–MgX no organohalogēnīda (R–X) un magnija metāla (Mg), parasti ēteru šķīdinātājā (piemēram, dietilēterā vai THF);
- R–MgX kā nukleofils pievienojas karbonilgrupai (C=O), veidojot alkoksīda–magnija kompleksu (R–C(OMgX)–Rʹ);
- Skāba apstrāde (piemēram, H3O+) hidrolizē Mg–O saiti un atbrīvo gala produktu — alkoholu, ja sākotnējais substrāts bija aldehīds vai ketons. Ja substrāts ir CO2, pēc darba uzdonešanas rodas karbonskābe.
Jāņem vērā, ka oglekļa‑magnija saite ir ļoti polāra ar lielu karbanjonam līdzīgu raksturu, tāpēc Grignarda reaģenti ir gan spēcīgas bāzes, gan spēcīgi nukleofili.
Grignarda reaģentu iegūšana un nosacījumi
Grignarda reaģentu parasti sagatavo, reaģējot alkil‑ vai arilhalogenīdu ar magniju metālu ētera šķīdinātājā. Lai panāktu veiksmīgu reaģenta veidošanos, bieži izmanto magnija virsmas aktivizāciju (piemēram, žilete, joda kristāli, ultraskaņa vai ķīmiska aktivizācija). Izplatītas praktiskas prasības:
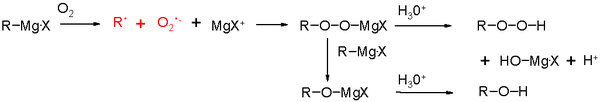
- Ekstremāla mitruma un skābekļa izslēgšana — sausas kolbas, liesmas žāvēšana, reakcijas veikšana inertajā atmosfērā (slāpeklis vai argons);
- Šķīdinātāji: dietilēters vai tetrahidrofurāns (THF), kas stabilizē Grignarda reaģentu esošo metālorganisko klasteru formu;
- Halogenīda reaktivitāte: jodīdi > bromīdi > hlorīdi, tāpēc ar alkilhlorīdiem reaģenti veidojas grūtāk;
- Ultraskaunas un citi aktivizācijas paņēmieni var palīdzēt noņemt adsorbēto mitrumu uz magnija virsmas un uzsākt reakciju.
Praktiskie ierobežojumi un drošība
Galvenie Grignarda reaģentu ierobežojumi un bīstamības faktori:
- Jutība pret protiskiem šķīdinātājiem un funkcionālajām grupām: Grignarda reaģenti reaģē ar ūdeni, alkoholiem, amīniem, karboksilskābēm, tioliem utt., tādējādi tos deaktivizējot. Atmosfēras mitrums samazina iegūstamo reaģentu iznākumu. Lai to novērstu, laboratorijās parasti izmanto sausas kolbas un inertu gāzi, kā arī žāvē šķīdinātājus.
- Reakcijas nekompatibilitāte: substrāti, kuri paši satur reakcīvas protiskas vai reducējošas grupas, nav piemēroti bez iepriekšējas grupu aizsardzības;
- Sānu reakcijas: iespējama Wurtza tipa coupling (R–R) starprekcija vai redukcija (veidojot alkanus), īpaši, ja nav rūpīgas kontroles par reaktantu attiecībām un temperatūru;
- Reaģenta agregācija: Grignarda reaģenti bieži pastāv kā dimeri vai lielāki klasteri, sasaistīti ar ētera molekulām, kas ietekmē reaktivitāti;
- Drošība: Grignarda reaģenti ir ļoti reaktīvi un var degt vai spontāni reaģēt ar ūdeni, tāpēc tos izmanto rūpīgi un ar atbilstošām aizsargierīcēm.
Pielietojums organiska sintēzē
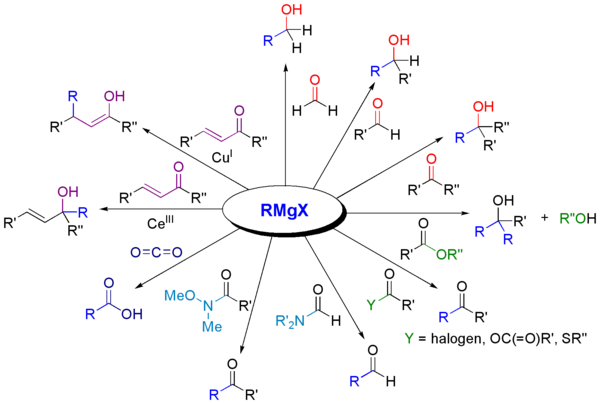
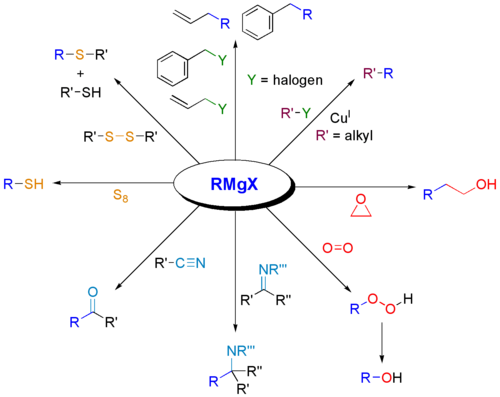
Grignarda reakcija ir viens no pamatinstrumentiem organiskajā sintēzē. Tipiskie pielietojumi:
- Alkoholu sintēze — pievienojot Grignarda reaģentu aldehīdiem un ketoniem, iegūst primāros, sekundāros vai terciāros alkoholus pēc skābas apstrādes;
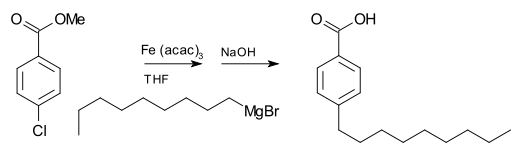
- Karbonskābju iegūšana — reakciója ar CO2 seko skābas apstrāde, kam seko karbonskābe;
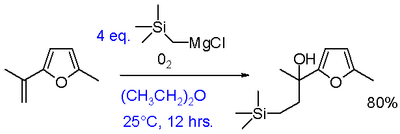
- Citālo funkcionālo grupu sintēze — piemēram, veidojot silylētu, borētus vai fosforētus atvasinājumus ar attiecīgiem reagentiem;
- Starpprodukts daudziem organiskajiem sintēzes ceļiem, tostarp farmaceitisku un smaržvielu ražošanā;
- Grignarda reaģenti var tikt izmantoti arī kā reagenti ķīmiskajos pārvietojumos un kombinācijās ar pārejas metālu katalizētām reakcijām.
Mehāniska piezīme un bieži jautājumi
Svarīgi praktiski fakti: Grignarda reaģents ir ļoti bāzisks (konjugātā skābe — alkanu C–H — pKa ir apmēram 45). Tas nozīmē, ka jebkura viegli protiska slāņa klātbūtne iznīcinās reaģentu, tāpēc reakcija ir praktiski neatgriezeniska attiecībā uz protonu pievienošanu. Neraugoties uz plašo izmantojumu, Grignarda reaģenti parasti neveido oglekļa–oglekļa saišu ar alkilhalogenīdiem vienkāršā SN2 ceļā ar labu iznākumu; tādas savienojumu veidošanas shēmas biežāk konkurē ar citām blakusreakcijām.
Vēsture
Grignarda reakcijas atklāja franču ķīmiķis Franču ķīmiķis Frānsuā Ogists Viktors Grignārs (François Auguste Victor Grignard). Par šo atklājumu un saistītiem pētījumiem viņam piešķīra Nobela prēmiju ķīmijā 1912. gadā. Reakcija un reaģenti viņa vārdā ir palikuši par vienu no organiskās sintēzes stūrakmeņiem.
Īsā secinājumā: Grignarda reakcija ir universāls un spēcīgs līdzeklis oglekļa–oglekļa saišu veidošanā, taču tās lietojumam nepieciešama laba eksperimentālā prakse, sausas un inertas vides nodrošināšana, kā arī uzmanība saderībai ar funkcionālajām grupām.