Cikloadikcija ir ķīmiska reakcija starp reaģējošām vielām ar dubultsaitēm, kas tiek aizstātas ar gredzena struktūru. Tā ir pericikliska ķīmiska reakcija, kurā "divas vai vairākas nepiesātinātas molekulas (vai vienas un tās pašas molekulas daļas) apvienojas, veidojot ciklisko aduktu, kurā notiek neto saites daudzuma samazināšanās". Tā ir ciklizācijas reakcija: tā veido jaunu atomu gredzenu.
Cikloadikācijas sauc pēc to molekulu pamatizmēra, kuras tiek savienotas. Tādējādi Dilsa-Aldera reakcija būtu [4 + 2]cikloadikcija, bet 1,3-dipolārā cikloadikcija - [3 + 2]cikloadikcija. Šāda veida reakcija ir nepolāra pievienošanas reakcija.
Paplašināts skaidrojums
Cikloadikcija parasti norisinās kā pericikliska, t.i., koncertēta elektronu pārvietošanās pa noslēgtu gredzenu pārejas stāvokli. Tas nozīmē, ka saites veidošanās un sadalīšanās notiek vienlaikus, bez parciālas vienas saites garozas starpposma. Tomēr pastāv arī pakāpeniskas vai radikālas alternatīvas, īpaši, ja reakcijas ķēde ir elektroniski vai steriski pakļauta šķelšanai.
Klasifikācija un piemēri
- [4 + 2] cikloadikcijas — klasiskais piemērs ir Dilsa-Aldera reakcija, kas savieno dīēnu (4 π-elektroni) un dienofilu (2 π-elektroni), veidojot sešcilindru gredzenu.
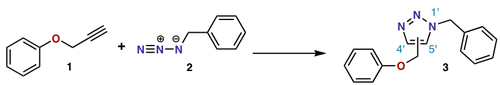
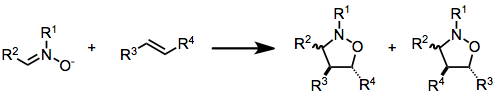
- [3 + 2] cikloadikcijas — 1,3-dipola cikloadikcijas, piemēram, azomethīna ylide vai nitriloksīdu pievienošanās, veido piecu locekļu gredzenus.
- [2 + 2] cikloadikcijas — parasti termiski aizliegtas kā koncertētas reakcijas (sakarā ar orbītu simetriju), bet var norisināties fotokemiski vai caur stepwise mehānismiem.
- Hetero-cikloadikcijas — ja vienā vai abos reaģentos ir heteroatomi (O, N, S), rodas heterocikliskie produkti.
- Intramolekulāras cikloadikcijas — reaģenti ir vienā molekulā, kas bieži vada ātru un stereospecifisku gredzenu veidošanos (piem., makrocikli vai daudzcikliskas struktūras).
Orbītu simetrija un Woodward–Hoffmann noteikumi
Cikloadikcijas bieži izskaidro, izmantojot Frontier Molecular Orbital (FMO) teoriju un Woodward–Hoffmann orbītu simetrijas principus. Galvenais arguments ir, vai reakcijas nozīmīgākās orbītas (HOMO un LUMO) mijiedarbojas tā, lai pārejas stāvoklis būtu simetrijiski atļauts. Piemēram:
- [4 + 2] termiski koncertēts ceļš parasti ir atļauts (suprafacial pieeja dienam) — tāpēc Dilsa-Aldera reakcijas termiski notiek viegli.
- [2 + 2] termiski suprafacial → suprafacial ceļš ir orbītiāli aizliegts, bet fotokemiski ekscitācija var mainīt orbītu aizpildījumu un ļaut reakcijai noritēt.
- Suprafacial vs antarafacial — attiecas uz to, kā elektronu bloki pievienojas pie dubultsaites virs/zem molekulas plāna; lielākajās organiskajās molekulās antarafacial pieeja ir steriski neizpildāma, tādēļ reakcijas bieži nav iespējamas bez fotonikas vai īpašiem apstākļiem.
Stereoķīmija un reģio-izvēle
Cikloadikcijas parasti ir ļoti stereospecifiskas un bieži saglabā sākotnējo dublētu saišu konfigurāciju produktā. Tipiski aspekti:
- Endo/Exo selektivitāte Dilsa–Aldera reakcijās — endo-produkti bieži dominē termiskajos nosacījumos (Alder endo likums), jo tie izmanto papildu sekundāras orbītu mijiedarbības.
- Regioselectivitāte (kāda daļa viena reaģenta savienojas ar kuras daļas otru) prognozējama, izmantojot FMO — elektronbagātīgie un elektroniem pievilcīgie substituenti nosaka, kur notiks pievienošanās.
- Ar enantiomēru selektivitāti var panākt, lietojot ķirālus katalizatorus (piem., ķirālas Lewis skābes), kas ir svarīgi farmaceitisko savienojumu sintēzē.
Katalīze, nosacījumi un praktiskie aspekti
- Lewis skābes (AlCl3, BF3, TiCl4 u.c.) bieži paātrina Dilsa–Aldera un citus cikloadikcijas, pazeminot dienofila LUMO enerģiju.
- Dažkārt izmanto fotokemiju, lai aktivizētu reakciju, īpaši, ja termiski koncertēts ceļš ir orbītiāli aizliegts.
- Solventi: izvēle ietekmē reakcijas ātrumu un selektivitāti — nepolāri vai viegli polarizējami šķīdinātāji ir bieži lietoti, bet polaritāte var mainīt FMO mijiedarbību.
- Temperatūra: zemākas temperatūras var palielināt stereoselektivitāti (mazāks termisku reakciju konkurences efekts), bet augstāka temperatūra var veicināt termiski aizliegtu alternatīvu mehānismu vai reversibilitāti.
Pielietojums un nozīme sintēzē
Cikloadikcijas ir vienas no fundamentālākajām metodēm gredzenu veidošanai organiskajā sintēzē. Tās plaši izmanto:
- dabisko produktu un farmaceitiski aktīvu vielu sintēzē (ļoti efektīvi veido sarežģītus cikliskus skeletus);
- polimēru ķīmijā (piem., cikloadīcijas veidošana kā savienošanas posms);
- materiālu ķīmijā un organiskajā elektronikas laukā (sintezējot funkcionālas molekulas ar specifiskām optiskām vai elektriskām īpašībām).
Ierobežojumi un izaicinājumi
Galvenie ierobežojumi ir steriskā aizkave, elektroniska neatbilstība starp reaģentiem (nepietiekama HOMO–LUMO pārošanās), kā arī orbītu simetrijas aizliegumi, kas var padarīt reakciju termiski neiespējamu bez papildu aktivācijas. Dažkārt nepieciešami katalizatori, fotons excitācija vai izmaiņas molekulārā dizainā, lai panāktu vēlamo produktu un selektivitāti.
Kopumā cikloadikcijas ir jaudīgs un daudzpusīgs rīks organiskajā sintēzē, kas ļauj efektīvi un stereokontroli veidot dažādas cikliskās struktūras.
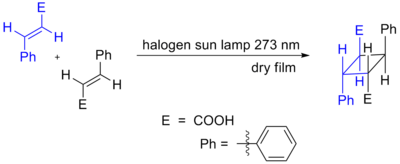
.png)
![Intermolecular Formal [3+3] Cycloaddition Reaction](https://www.alegsaonline.com/image/600px-3+3-cycloaddition.svg.png)