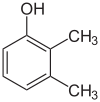
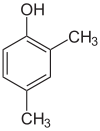
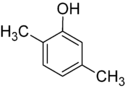
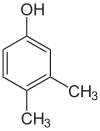
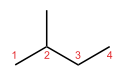Strukturālā izomērija (IUPAC to sauc par konstitucionālo izomēriju) ir izomērijas paveids, kurā divām ķīmiskajām vielām ir viena un tā pati molekulārā formula, bet molekulas ir savienojušās dažādās secībās (atšķiras atomu savienojumu kārtība). Strukturālajai izomērijai pretēja ir stereoizomērija — pēdējā rodas, ja viena un tā pati piesaistes secība saglabāta, bet atšķiras telpiska izvietojuma (konformācijas, konfigurācijas utt.).
Definīcija un galvenās īpašības
Konstitucionālie (strukturālie) izomēri ir savienojumi ar identisku summāro formulu, taču atšķirīgu atomu savienojumu secību. Tā kā saites savienojumi ir citi, šiem izomēriem parasti ir atšķirīgas fiziskās un ķīmiskās īpašības — kušanas un vārīšanās temperatūras, šķīdība, reakciju specifika, spektrālas pazīmes (NMR, IR, MS utt.).
Veidi un piemēri
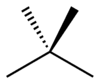
- Skeleta (ķēdes) izomēri — atšķiras oglekļa ķēdes uzbūve (taisna ķēde vs zarota ķēde).
Piemērs: C4H10 — n-butāns (CH3CH2CH2CH3) un izobutāns ((CH3)3CH). - Pozicionālie (regio) izomēri — funkcionālie grupas vai atomi ir pievienoti dažādās ķēdes pozīcijās.
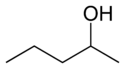
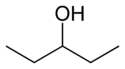
Piemērs: alkoholi C4H9OH — 1-butanols (OH pie pirmā oglekļa) un 2-butanols (OH pie otrā oglekļa). - Funkcionālie izomēri — satur atšķirīgas funkcionālās grupas, lai gan summārā formula ir vienāda.
Piemērs: C2H6O — etanols (CH3CH2OH) un dimetilēters (CH3OCH3). - Tautomēri — īpaša funkcionālo izomeru grupa, kas viegli pāriet viens otrā caur protonu migrāciju un dubultās saites rekonstrukciju.
Piemērs: keto–enola tautomerija (acetona enola forma pret acetonu), vai purīnveida savienojumu tautomērija. Tautomēri parasti veido dinamiski līdzsvaru, un dominējošā forma var atšķirties atkarībā no vides (šķīdinātājs, pH).
Kā atšķirt strukturālos izomerus
Lai noteiktu, kurš no strukturālajiem izomēriem ir klāt, izmanto vairākas metodes:
- NMR spektroskopija — 1H un 13C NMR sniedz informāciju par atomu vidi un savienojumu pozīcijām.
- IR spektroskopija — parāda funkcionālo grupu signālus (OH, C=O, C–O u.c.).
- Masu spektrometrija (MS) — fragmentācijas modeļi bieži atšķiras starp izomēriem.
- Fizikālās īpašības — salīdzinot kušanas/vārīšanās temperatūras, blīvumu, šķīdību, var gūt norādes.
- Kemiskā reaktivitāte — reakcijas produktu veids un kinētika var norādīt uz atšķirīgu funkcionālo grupu vai pozīciju.
Nozīme organiskajā ķīmijā un praktiskie piemēri
Strukturālā izomērija ir būtiska organiskajā ķīmijā, farmācijā, materiālzinātnē un rūpniecībā, jo mazās atšķirības molekulārajā savienojumā var radīt lielas izmaiņas bioloģiskajā aktivitātē, stabilitātē un fizikālajās īpašībās. Piemēram:
- Divi funkcionālie izomēri var atšķirties pēc toksicitātes vai terapeitiskā efekta.
- Zarotas ogļūdeņražu ķēdes var mainīt degvielas dedzināšanas īpašības.
- Tautomērija ietekmē reakciju mehānismus un reaģentu selektivitāti sintēzē.
Papildu piezīmes
Ar ogļūdeņražu atomu skaita pieaugumu iespējamais strukturālo izomeru skaits strauji palielinās — tāpēc sazarotu molekulu uzbūves inventarizācija un pareiza nosaukšana ar IUPAC sistemātiku ir svarīga. Strukturālā izomērija bieži tiek aplūkota kā pirmais līmenis, kad klasificē izomērus; turpmāk var sekot stereoizomērijas analīze, kad tiek spriests par telpisko konfigurāciju.