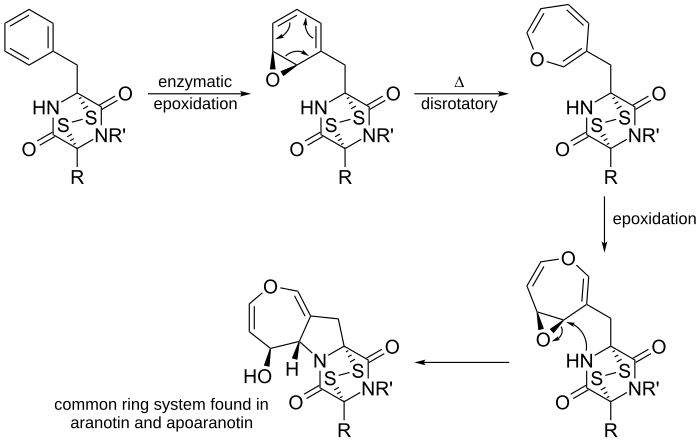
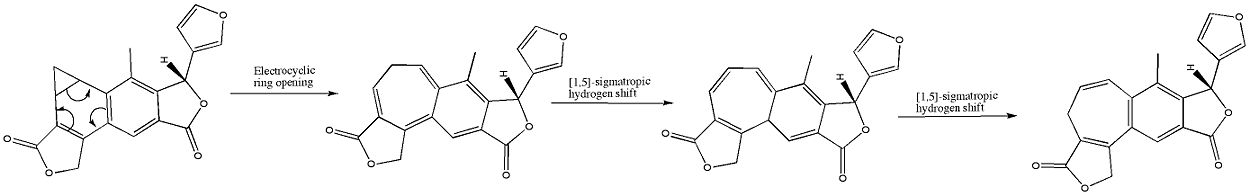
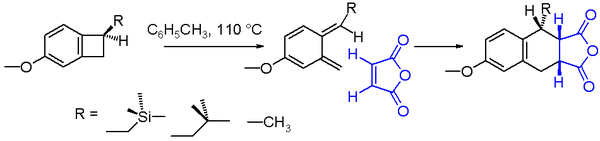
Organiskajā ķīmijā elektrocikliskā reakcija ir pericikliskās pārkārtošanās reakcijas apakškopa, kurā notiek koncertēta (bez starpproduktiem) saišu pārkārtošanās ap ciklisku molekulāro orbitāļu loku. Reakcija tiek dēvēta par elektrociklisku, ja tās rezultātā viena pi saite transformējas par vienu sigma saiti (gredzena noslēgšana) vai vienas sigma saites atvēršanās rada pi saites (gredzena atvēršana). Elektrocikliskajām reakcijām kopumā raksturīgas šādas īpašības:
- tās var tikt aktivizētas ar gaismu (fotoinducētas) vai ar siltumu (termiskas);
- reakcijas stereokemiju nosaka pi elektroniskā sistēma — īpaši to delokalizēto pi elektronu skaits tajā daļā, kurā ir vairāk pi saišu;
- elektrocikliskā pāreja var noslēgt gredzenu (elektrocikliska ciklizācija) vai atvērt gredzenu (gredzena atvēršanās);
- stereospecifiskumu nosaka, vai pārejas stāvoklī galapunkti pagriežas konrotatoriski vai disrotatoriski, kā paredz Vudvarda–Hofmana noteikumi;
- elektrocikliskajās reakcijās tiek saglabāta molekulāro orbitāļu simetrija (orbital symmetry conservation), ko paredz teorija un ko apstiprina eksperimentāli.
Vudvarda–Hofmana noteikumi (elektrocikliskām reakcijām)
Vudvarda–Hofmana noteikumi nosaka, kāda rotācijas veida (konrotatoriska vai disrotatoriska) izmantošana ir simetriski iespējama, ņemot vērā pi elektronu skaitu un attiecīgi vai reakcija notiek termiski vai fotoinducēti. Īsumā:
- Termiski (zemes stāvoklī):
- 4n pi elektroni (piemēram, 4 π) — konrotatoriska gredzena atvēršanās/veidošanās ir simetrijiski atļauta;
- 4n+2 pi elektroni (piemēram, 6 π) — disrotatoriska gredzena atvēršanās/veidošanās ir simetrijiski atļauta.
- Fotoinducēti (uzbudinātā stāvoklī):
- noteikumi apgriežas: 4n pi elektroni — disrotatoriski atļauta; 4n+2 pi elektroni — konrotatoriski atļauta.
Šie likumi izriet no orbītu fāžu sakritības HOMO (vai attiecīgā MO uzbudinātā stāvokļa) pārejas stāvoklī: tikai tad, ja gala p-orbitāļu fāzes atbilst produkta orbītālēm, pāreja notiek bez orbītu simetrijas pārkāpuma.
Mehānisms un orbītu skaidrojums
Elektrocikliskās reakcijas ir koncertētas pericikliskas pārejas, kur visas iesaistītās saišu pārkārtošanās norisinās vienlaicīgi caur ciklisku orbītu sadarbību. To skaidro izmantojot robežu (frontier) molekulāro orbītu metodi: reakcijas gaitā reaģenta HOMO fāzes un ģeometrijas konfigurācija nosaka, kura rotācijas reģistrējas (konrotatoriska vai disrotatoriska). Ja fāžu atbilstība ir labvēlīga, pāreja ir "simboliski atļauta" un tā noris ar salīdzinoši zemu enerģijas barjeru.
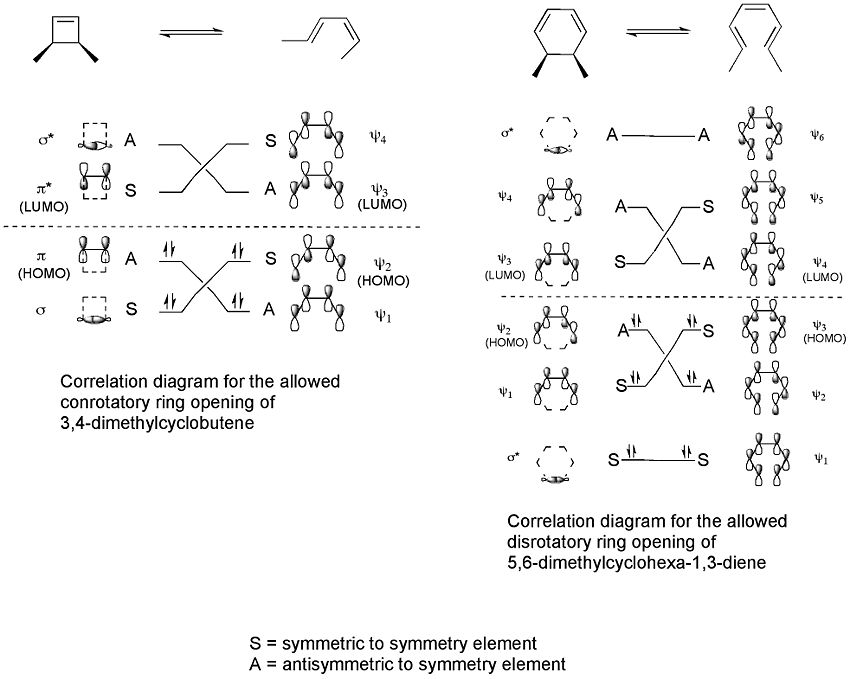
Vēl viens konceptuāls paņēmiens ir orbītu korelācijas diagrammas (orbital correlation diagrams), kas parāda, kā reaģentu orbitāļi korelē ar produkta orbitālēm, izskaidrojot simetrijas saglabāšanu pārejas ceļā.
Torkvoselektivitāte
Elektrociklisko reakciju stereokemija var ietekmēt torkvoselektivitāte — preferenciāla vienas vai otras rotācijas virziena izvēle, kas nosaka, kurš enantiomērs vai diastereomērs dominēs produktā. Lai gan konrotatoriska reakcija nosaka rotācijas relatīvus virzienus (abi galapunkti griežas vienā virzienā), aizvietotāji joprojām var rotēt iekšā vai ārā un šīs iespējas var būt enerģētiski nevienlīdzīgas. Torkvoselektivitātes iemesli:
- steriskas mijiedarbības (pieeja, kas izvairās no steriskas sadursmes);
- elektroniskas/supraorbītu mijiedarbības (pi- un sigma-orbītu sekundāras mijiedarbības, hiperkonjugācija);
- solventefekti un katalītiskie apstākļi (piem., kations veicina noteiktus ceļus, kā Nazarova reakcijā).
Praxis: torkvoselektīvas metodes ļauj sintēzēs iegūt produktus ar enantiomēru vai diastereomēru pārsvaru, kas ir svarīgi farmaceitiskajā sintēzē un stereoselektīvā organiskajā sintēzē.
Piemēri
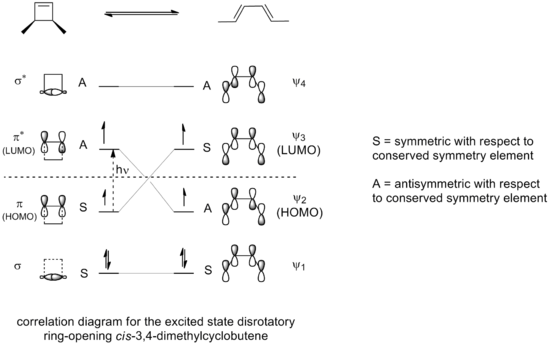
Tipisks un bieži citēts piemērs ir 3,4-dimetilciklobutēna termiskā gredzenveida atvēršanās. No cis izomēra tiek iegūts tikai cis,trans-2,4-heksadiēns, bet trans izomērs dod trans,trans-diēnu. Šīs rezultātu atšķirības izriet no tā, ka termiskā atvēršanās 4 π sistēmā notiek konrotatoriski, lai saglabātu HOMO fāžu atbilstību. Attēlā parādīts mehānisms un fāžu izkārtojums:
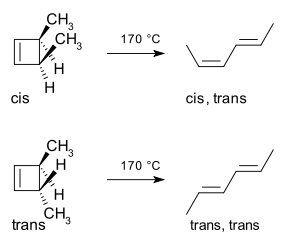
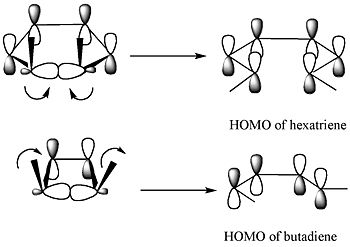
Nākamajā diagrammā redzama robežu orbītu metode, kas rādīta uz example of ring opening mechanism:
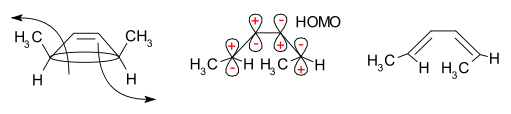
Vēl viens svarīgs piemērs ir Nazarova ciklizācija — elektrocikliska ciklizācija, kas noslēdz gredzenu un pārvērš divinilketonus par ciklopentenoniem. Šī reakcija noris kationiskā vidē (parasti skābes katalizēta) un būtībā ir 4π elektrociliskā ciklizācija, kuru plaši izmanto sintētiskajā ķīmijā, lai veidotu pieci locekļu ringus. (Reakciju atklāja Ivans Nikolajevičs Nazarovs (1906–1957).)
Praktiskā nozīme un pārbaude
Ķīmiķus interesē elektrocikliskās reakcijas, jo to stereokīmiskie rezultāti bieži apstiprina teorētiskās prognozes par orbītu simetriju. Eksperimentāli novērojumi — produktu stereokarakteristika, termisko vs fotoinducēto ceļu atšķirības un torkvoselektivitātes efekti — sniedz spēcīgu atbalstu orbītu simetrijas saglabāšanas principam.
Elektrocikliskās reakcijas ir plaši izmantotas organiskajā sintēzē, jo tās ļauj konstruēt ciklus ar augstu stereokontroli un bez nepieciešamības pēc starpproduktiem. Pareiza elektronu skaita, temperatūras/uzbudinājuma un aizvietotāju izvēle ļauj plānot reakciju stereokemiju un iegūt vēlamo konformāciju un konfigurāciju.
Rezuments
Elektrocikliskās reakcijas ir fundamentāla pericikliskā procesu klase, kuras stereokemiju un iespējamību nosaka pi elektronu skaits un Vudvarda–Hofmana noteikumi. Izpratne par orbītu fāzēm, torkvoselektivitāti un ārējā apstākļu ietekmi ļauj paredzēt un kontrolēt šīs reakcijas sintētiskajā praksē.