Reakcija NS1 ir aizvietošanas reakcija organiskajā ķīmijā. "SN" apzīmē nukleofīlo aizvietošanu, un "1" norāda, ka ātrumu noteicošajā solī piedalās tikai viena molekula (vienmolekulāra). Reakcijā rodas karbokācijas starpprodukts. Dažas bieži sastopamas NS1 reakcijas ir sekundāro vai terciāro alkilhalogenīdu reakcijas ar sekundārajiem vai terciārajiem alkoholiem vai ar bāzēm/skatījumiem, kā arī tercīāro alkilhalogenīdu reakcijas skābos vai protiskos šķīdinātājos. Ar primārajiem alkilhalogenīdiem parasti notiek alternatīva <sub>N</sub>S2 reakcija. Neorganiskās ķīmijas speciālistu vidū NS1 mehānismu bieži dēvē par disociatīvo mehānismu. Kristofers Ingolds un citi pirmo reizi ierosināja šāda mehānisma aprakstu 1940. gados.
Mehānisms — divi soli
NS1 mehānisms parasti sastāv no diviem pamatsoļiem:
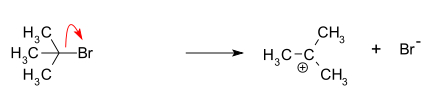
- 1. solis (ātrumu noteicošais): substrāts (R–LG) disociē, atdalās labais atstājējs (LG–), veidojot karbokāciju (R+). Šis solis ir lēnākais un nosaka reakcijas ātrumu.
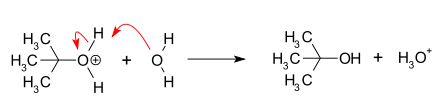
- 2. solis: nukleofīls (Nu) ātri reaģē ar karbokāciju, veidojot aizvietoto produktu (R–Nu).
Faktori, kas veicina NS1
- Substrāta struktūra: karbokācijas stabilitāte ir izšķiroša — terciārie > sekundārie > primārie. Resonansi stabilizēti karbokācijas (piem., benzil- vai alil-karbokācijas) arī viegli veidojas.
- Atstājējgrupa: laba atstājējgrupa (piem., I–, Br–, TsO–) padara jonizāciju vieglāku un veicina NS1.
- Šķīdinātājs: polāri protiski (piem., ūdens, alkoholi) stabilizē jonu pārus un samazina aktivācijas enerģiju, tādējādi veicinot dissociāciju.
- Nukleofīla spēks: pretēji NS2, spēcīgs nukleofīls nav nepieciešams; vāji nukleofili (ūdens, spirtos) var viegli uzbrukt karbokācijam.
- Temperatūra un šķietamās konkurences reakcijas: augstāka temperatūra veicinās elimināciju (E1) no tāda paša karbokācijas starpprodukta, tāpēc nosacījumi ietekmē produktu sadalījumu.
Stereohēmija un joniskie pāri
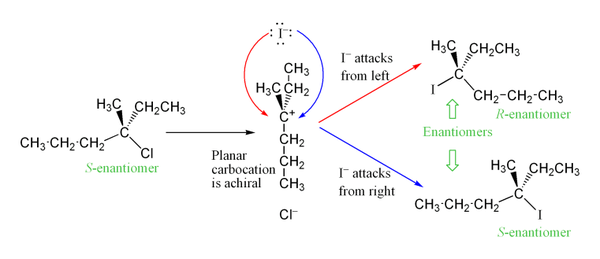
Karbokācijas ir sp2 hibridizētas un plakanas, tāpēc uzbrukums no divām pusēm parasti noved pie racemizācijas (ja sākotnējā centrs bija kirāls). Taču eksperimentā bieži tiek novērota daļēja racemizācija vai neliels stereokontrols, jo reakcijas laikā var pastāvēt joniskais pāris (t.i., atstājēja anjons tuvu karbokācijam), kas ierobežo piekļuvi vienai pusei un var dot nelielu inversiju vai preferenci.
Karbokāciju pārbīdes (rearrangements)
Karbokācijas var pārkārtoties, ja iespējama stabilāka karbokācija (piem., hidrīda vai metilgrupu pārvietošanās). Šīs pārbīdes bieži izskaidro negaidītus produktus: sākotnējais aizvietojums var būt novērojams uz citā oglekļa atomā nekā tas, kur attiecīgais atstājējs sākotnēji atradās.
Piemēri
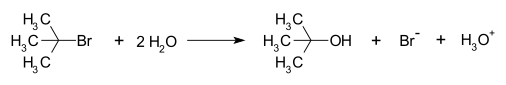
- Terciārais halogenīds: 2‑metil‑2‑propanilhlorīds (tert‑butilhlorīds) + ūdens → tert‑butilspirts. Šī ir klasiska NS1 solvolīzes reakcija, kur pirmkārt veidojas tert‑butilkarbokācija, kura pēc tam reaģē ar ūdeni.
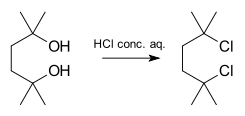
- Terciārs spirts skābos apstākļos: terc‑butanols + HCl → terc‑butilhlorīds. Proti, protonēts alkohols atstāj kā ūdens molekula, veidojot karbokāciju, kam seko halogēna anjona pievienošanās.
- Benzil/Alil sistēmas: benzilhalogenīdi un alilhalogenīdi viegli stabilizē karbokāciju ar rezonansi, tāpēc tos bieži skar NS1 mehānismi pat tad, ja centrsi nav terciāri.
Konkurence ar E1 un NS2
Pie tādām pašām sākotnējām nosacījumiem NS1 bieži konkurē ar E1 (elimināciju) — abas izmanto karbokācijas starpproduktu. Augstāka temperatūra, vājāki nukleofili un bāziskāki apstākļi palielina eliminācijas iznākumu. Ar primārajiem substrātiem biežāk notiek NS2, nevis NS1.
Eksperimentālie pierādījumi un diagnostika
- Kinetika: reakcijas ātruma atkarība no substrāta koncentrācijas (pirmās pakāpes) un neatkarība no nukleofīla koncentrācijas ir spēcīgs NS1 rādītājs.
- Stereokīmija: daļēja vai pilnīga racemizācija liecina par plakanas karbokācijas starpproduktu.
- Hammett un citos mehāniskajos pētījumos: pozitīvas attiecības ar substitūciju, kas stabilizē pozitīvo lādiņu, un šķīdinātāju ietekme atbilst jonu veidošanās modelim.
Praktiski padomi laboratorijā
- Lai veicinātu NS1: izmantojiet polāru protisku šķīdinātāju, labu atstājējgrupu un substrātus, kuros var veidoties stabils karbokācijas.
- Sagaidāmas pārbīdes un konkurējoša eliminācija — analizējiet produktus ar GC/GC‑MS vai NMR, lai noteiktu, vai notikušas pārstrukturēšanas vai eliminācijas ceļu produkti.
Kopsavilkumā: NS1 ir disociatīvs mehānisms, kur ātrumu nosaka vienas molekulas jonizācija līdz karbokācijas veidošanās, un tā iznākums spēcīgi atkarīgs no karbokācijas stabilitātes, atstājējgrupas un šķīdinātāja īpašībām. Praktiķiem jāņem vērā arī iespējamās pārbīdes un konkurējošās E1 reakcijas.