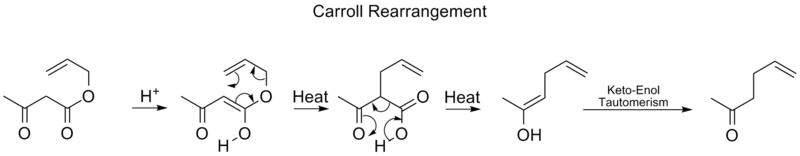
Sigmatropiska reakcija organiskajā ķīmijā ir pericikliska reakcija. Sigmatropiskajā reakcijā neizmanto katalizatoru, un tajā piedalās viena molekula (nekatalizēts intramolekulārs process). Tā maina vienu σ saiti uz citu σ saiti. Nosaukums sigmatropiskā reakcija radies, apvienojot sen zināmo "sigma" nosaukumu, kas apzīmē atsevišķas oglekļa-oglekļa saites, un grieķu vārdu tropos, kas nozīmē pagrieziens. Tā ir pārkārtošanās reakcija, kas nozīmē, ka molekulas saites pārvietojas starp atomiem, neatstājot nevienu atomu un nepievienojot molekulā jaunus atomus. Sigmatropiskajā reakcijā aizvietotājs pārvietojas no vienas π saišu sistēmas daļas uz citu daļu, veicot intramolekulāru reakciju ar vienlaicīgu π sistēmas pārkārtošanos. Īstām sigmatropiskām reakcijām parasti nav nepieciešams katalizators. Dažas sigmatropiskās reakcijas katalizē Lūisa skābe. Sigmatropiskajām reakcijām bieži ir pārejas metālu katalizatori, kas veido starpproduktus analogās reakcijās. Vispazīstamākās sigmatropiskās pārkārtošanās reakcijas ir [3,3] Kope pārkārtošanās, Klaisena pārkārtošanās, Kerola pārkārtošanās un Fišera indola sintēze.
Kas ir sigmatropiska reakcija — īsumā
Sigmatropiska reakcija ir pericikliska, parasti koncertēta intramolekulāra pārkārtošanās, kurā viena σ saite migrē pa π saišu sistēmai, izraisot saikšu pārorientāciju un jaunu saikšu veidošanos molekulā bez atomu zuduma vai pievienošanas. Šāda veida reakcijas ir bieži stereospecifiskas un notiek caur ciklisku pārejas stāvokli.
Mehānisms un elektroniskā skaidrošana
Mehānisms parasti ir koncertēts (visi elektroni pārvietojas vienlaikus) un tiek aprakstīts kā pericikliska pārejas stāvokļa veidošanās. Svarīgākie principi:
- Reakcija iet caur ciklisku pārejas stāvokli, kur π elektroni un migrujošā σ saite veido periciklisku elektronu kustības loku.
- Woodward–Hoffmann noteikumi (orbitalu simetrijas saglabāšana) nosaka, kuri sigmatropiskie pārvietojumi ir termiski vai fotoķīmiski ļauti (allowed) un kuri ir aizliegti (forbidden) bez alternatīviem ceļiem vai katalizācijas.
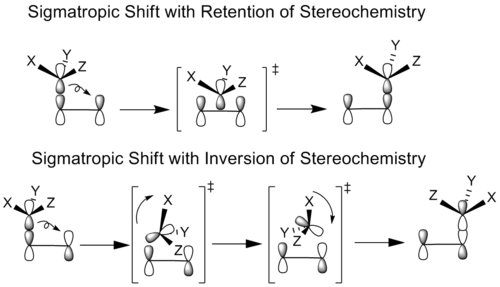
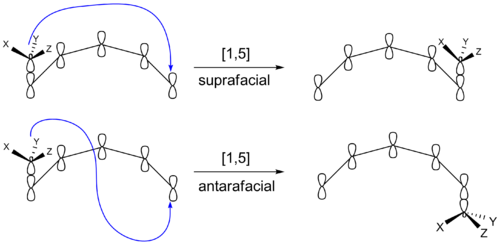
- Topoģija: migrācija var notikt suprafaciāli (no tās pašas π sistēmas sejas) vai antarafaciāli (no pretējām sejām). Tas ietekmē stereokemiju gala produktā.
Stereokīmija un allowed/forbidden reakcijas
Svarīga sigmatropisko pārvietojumu īpašība ir stereospecificitāte — veids, kā σ saite pārvietojas (suprafaciāli vai antarafaciāli), nosaka, vai saglabājas vai tiek mainīta konfigurācija ap centriem. Woodward–Hoffmann noteikumi nosaka, vai konkrēta sigmatropiska pāreja ir termiski pieļaujama kā koncertēts suprafaciāls process vai vai ir nepieciešama antarafaciāla kustība vai fotoaktivācija. Piemēram, daudzas [3,3]-pārkārtošanās (kaudzu populāru piemēru pamatā) termiski noris kā suprafaciālas un ir stereospecifiskas.
Bieži sastopami sigmatropisko reakciju tipi un piemēri
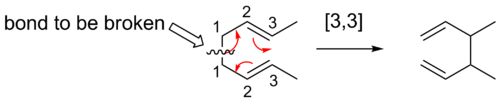
- [3,3] pārkārtošanās — ļoti izplatīta klase, kuras piemēri:
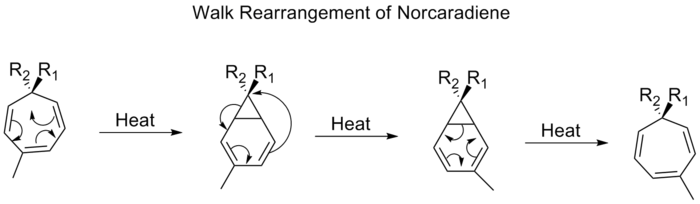
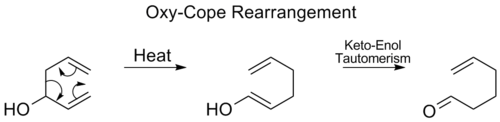
- Kope (Cope) pārkārtošanās: 1,5-dienu sistēmu pārkārtošanās, bieži termiska un reversīva.
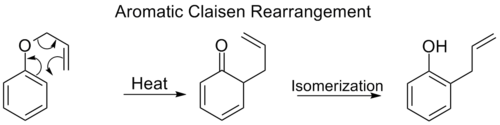
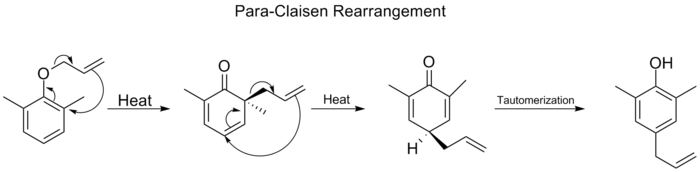
- Klaisena (Claisen) pārkārtošanās: allyl vinil ēteri → γ,δ‑nenosātināti aldehīdi/ketoni vai citas produktu grupas; ļoti noderīga sintezē ar stereokontroli.
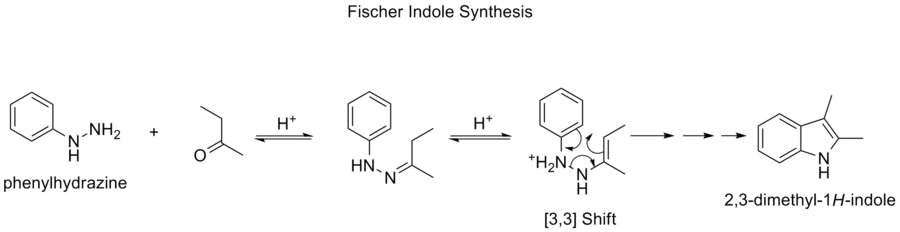
- Fišera (Fischer) indola sintēze — satur pārejas posmus, kas bieži ietver periciklusku pārkārtošanos (tajā skaitā [3,3] tipa elementus) un parasti tiek katalizēta ar skābēm.
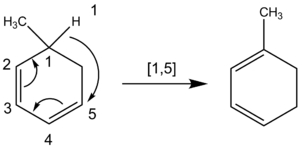
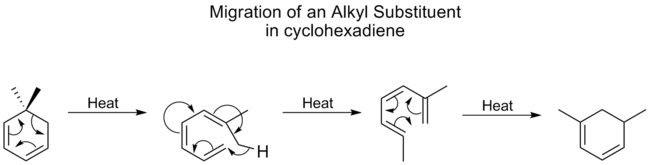
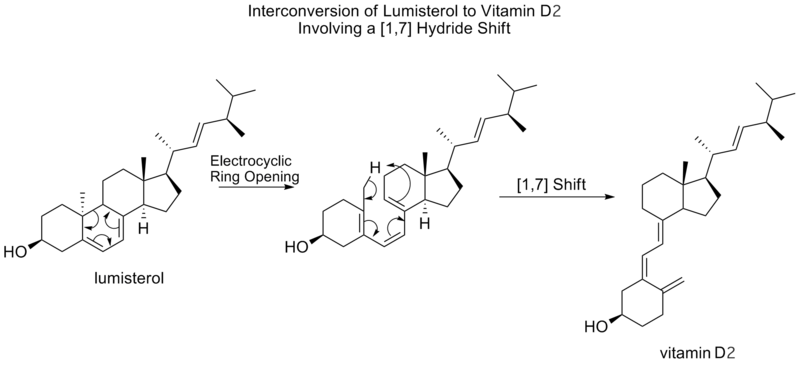
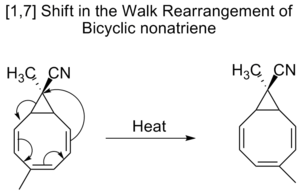
- [1,5]-hidrogēna pārvietojums — parastais piemērs ir 1,5‑H-shifts konjugētās sistēmās; šie šķērsojumi bieži ir termiski pieļaujami un stereospecifiski.
- [2,3] sigmatropiska pārvietošana — piemēram, sulfonoksīdu un ēteru [2,3]-pārkārtošanās (Wittig tipa un sānu reakcijas), kas dod stereospecifiskus produktus un tiek izmantotas sintezē.
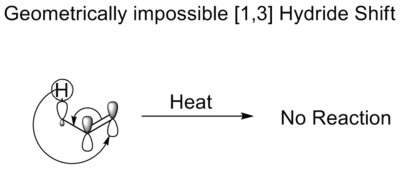
- Citādi piemēri — pastāv arī retos gadījumos [1,3] pārvietojumi, kuri parasti termiski ir aizliegti kā koncertēti procesi un bieži notiek caur radikālu vai jonu starpposmu.
Katalīze un alternatīvi mehānismi
Lai gan daudzas sigmatropiskās reakcijas ir termiski bezkatalizatoriskas, Lūisa skābe un citi katalizatori var samazināt pārejas stāvokļa enerģiju, mainīt reakcijas ceļu vai palielināt reakcijas ātrumu. Pārejas metāli dažkārt veicina līdzīgas pārkārtošanās caur koordināciju un starpproduktiem, kas locītās pericikliskās shēmas gadījumā atšķiras no koncertētā mehānisma, taču praktiķiem tie nodrošina vairāk iespēju retrosintētiskā plānošanā.
Praktiskā nozīme un lietojumi
Sigmatropiskās reakcijas ir svarīgas organiskajā sintēzē, jo tās ļauj izveidot sarežģītas sasaitēšanas shēmas un veidot stereokontrolētus produktus bez ārējas pievienošanas. Tos izmanto dabisko produktu sintēzē, farmaceitiskajā ķīmijā un materiālu ķīmijā. Izvēloties piemērotu sigmatropisku pārkārtošanos, ķīmiķi var pārvietot funkcionālās grupas molekulā, saglabājot kopējo atomu skaitu un bieži iegūstot produktus augstā stereokvalitātē.
Īss kopsavilkums
Sigmatropiskas reakcijas ir pericikliska intramolekulāra pārvietošanās, kurā σ saite migrē pa π sistēmu, parasti koncertētā veidā. Tās ir stereospecifiskas, to noturību un iespējamību nosaka orbitalu simetrija (Woodward–Hoffmann principi), un tās ir plaši izmantotas organiskajā sintēzē. Pazīstamākie piemēri: Cope un Claisen pārkārtošanās, [1,5]-hidrogēna pārvietojumi, kā arī dažas sarežģītākas sintēzes kā Fišera indola sintēze.

![[1,3] Alkyl Shifts](https://www.alegsaonline.com/image/550px-1,3alkylfixed.png)
![[1,5] Hydride shift in a cyclic system](https://www.alegsaonline.com/image/300px-1,5hydridecyclicfixed.png)
![Antarafacial [1,5] Hydride Shift](https://www.alegsaonline.com/image/600px-1,5hantarafacialfixed.png)


![[5,5] shift of phenyl pentadienyl ether](https://www.alegsaonline.com/image/800px-5,5shiftfixeds.png)